- Gregor Lindner
- Martin Windpessl
- Markus Pirklbauer
- Sara H. Ksiazek
- Alexander Kirsch
- Roland Edlinger
- Marcus D. Säemann
März 2026
Konsensusempfehlungen zur Diagnose und Therapie der Hyperkaliämie der Österreichischen Gesellschaft für Nephrologie 2026
Autor:innen

Zusammenfassung
Eine Hyperkaliämie ist eine potentiell lebensbedrohliche Störung des Elektrolythaushaltes, welche deshalb eine rasche Diagnostik und Therapie notwendig macht. Während Hyperkaliämien in der Allgemeinbevölkerung selten auftreten, steigt das Risiko in Abhängigkeit von Komorbiditäten wie chronischer Nierenerkrankung, Diabetes mellitus oder Herzinsuffizienz deutlich an. Dabei spielt auch die Behandlung dieser Erkrankungen mit Medikamenten, welche das Renin-Angiotensin-Aldosteron-System beeinflussen, eine große Rolle. Die Therapie der Hyperkaliämie beruht einerseits auf Maßnahmen, um mögliche Störungen des
Herzreizleitungssystems zu behandeln und andererseits den Transport von Kalium in den Intrazellularraum zu
stimulieren sowie die Kaliumelimination zu erhöhen. Wichtig ist zudem das rasche Erfassen von klinischen
Situationen wie Fieber, Diarrhö, u.a., die bei Risikopatient:innen zu schweren Hyperkaliämien führen können, um rechtzeitig präventive Maßnahmen setzen zu können.
Definitionen
Eine Hyperkaliämie kann angelehnt an die Definition der Kidney Disease Improving Global Outcomes (KDIGO) als ein Wert über dem oberen Referenzwert für die Kaliumkonzentration im Plasma oder Serum [S‑K+] angesehen werden [1]. Der entsprechende Referenzwert für die [S‑K+] kann von Labor zu Labor variieren, wird aber oft mit 3,5–5,0 mmol/l angegeben (für die Plasma-Kaliumkonzentration bei ca. 3,4–4,5 mmol/l) [2, 3].
- Kalium Umrechnung g/mmol: 1 g = 25,6 mmol
Klassifikation
Der Schweregrad einer Hyperkaliämie wird auf Basis einer Expertenempfehlung in 3 Stadien, von mild bis schwer eingeteilt [1]. Die Einteilung basiert einerseits auf der absoluten Höhe der [S‑K+] und andererseits auf dem Vorliegen von Hyperkaliämie-assoziierten EKG-Veränderungen als Ausdruck einer schweren Gesundheitsgefährdung (Abb. 1; [1, 4]).

Kommentar
Aufgrund der geringen Sensitivität der EKG-Veränderungen unterliegt diese Einteilung erheblichen Limitationen (s. EKG-Veränderungen bei schwerer Hyperkaliämie) [5, 6].
Epidemiologie der Hyperkaliämie
Die Prävalenz der Hyperkaliämie wird in einer breiten Allgemeinpopulation mit 1,5–2,5 % angegeben, wenn als Grenze eine [S‑K+] von ≥ 5,0 mmol/l angenommen wird [7, 8]. Bei Notfallpatient:innen wurde die Prävalenz einer Hyperkaliämie bei gleicher Definition mit 3,6 % beschrieben [9]. Die Häufigkeit der Hyperkaliämie ist abhängig von Komorbiditäten, v. a. chronische Nierenkrankheit (CKD), Herzinsuffizienz (HF) oder Diabetes (DM) und von der Einnahme von Medikamenten, v. a. mit Wirkung auf das Renin-Angiotensin-Aldosteron-System (RAAS) (s. Tab. 1). Oft liegen mehrere dieser Faktoren gleichzeitig vor [10].

Bei Patient:innen mit Hypertonie ohne weitere Risikofaktoren werden nach Beginn einer Medikation mit einem RAAS-Inhibitor (RAASi) Inzidenzen einer Hyperkaliämie von > 5,0 mmol/l mit unter 5 % und > 5,5–6,0 mmol/l mit unter 2 % angegeben [11, 12]. Dies gilt auch für neuere Medikamente mit Einfluss auf das RAAS wie nichtsteroidale Mineralokortikoidrezeptorantagonisten (ns-MRA; z. B. Finerenon), Aldosteronsynthasehemmer (ASI), Zilebesiran, Sparsentan oder Aliskiren [13‐18].
Bestehen zusätzliche Risikofaktoren (s. unten), so ist bei 5–10 % der Patient:innen unter einer Monotherapie mit RAASi mit einer Hyperkaliämie zu rechnen [11, 19‐22]. Bei der Kombination von mehreren RAASi in den Risikopopulationen (CKD ± DM oder CKD ± HF) kann das Risiko einer Hyperkaliämie 10 % übersteigen [23‐29]. Bei diesen Patient:innen sind auch schwere Hyperkaliämien (> 6,0 mmol/l) häufiger zu beobachten (> 5 %) [29, 30]. Das Risiko für eine Hyperkaliämie unterscheidet sich bei Patient:innen mit HF nicht wesentlich zwischen „alten“, steroidalen MRA und ns-MRA, wenn diese mit ACEi/ARB kombiniert werden (12–16 %); ist aber mit ns-MRA deutlich niedriger bei Patient:innen mit Hypertonie oder Diabetes und (milder) Nierenfunktionseinschränkung [31‐33].
Bei Patient:innen mit höhergradig eingeschränkter Nierenfunktion (CKD G4–5) können Hyperkaliämien mit/ohne RAASi bei mehr als 50 % der Patient:innen auftreten [34]. Die Abb. 2 stellt das Hyperkaliämierisiko in verschiedenen Risikokonstellationen dar.
![Abb. 2 Risiko einer Hyperkaliämie in Abhängigkeit von unterschiedlichen Risikofaktoren. Die Abbildung zeigt näherungsweise die Prävalenzraten einer Hyperkaliämie ([S‑K+] > 5,5 mmol/l) anhand einer Auswahl von verschiedenen Studien mit unterschiedlichen Risikofaktoren und RAAS-Interventionen. Es wurden sowohl Interventionsstudien als auch Observationsstudien mit unterschiedlichen Beobachtungszeiträumen und unterschiedlicher Medikamentendosierung verwendet. Andere, hier nicht angeführte Studien können zum Teil auch höhere Prävalenzraten zeigen, was zum Teil an längeren Beobachtungszeiträumen liegt. HT Hypertonie, DM Diabetes mellitus, HF Herzinsuffizienz, CKD chronische Nierenerkrankung, TMP Trimethoprim, CNI Calcineurininhibitoren, NSAR nichtsteroidale Antirheumatika, AKI akute Nierenerkrankung, ASI Aldosteronsynthaseinhibitoren. Literatur zu den einzelnen Boxen: Box 1 [15, 20, 21, 23, 35‐37], Box 2 [24, 36], Box 3 [16‐18, 38‐41], Box 4 [26, 42], Box 5 [29, 39], Box 6 [38, 43, 44], Box 7 [27] und Box 8 [34]](https://cdn.prod.website-files.com/62a1addc5dabff015c15ef63/69b9e19b3b7097dac87afa55_508_2026_2708_Fig2_HTML.jpeg)
Auch akute Nierenfunktionseinschränkungen (AKI) sind häufig von einer Hyperkaliämie begleitet (Prävalenz von > 10–20 %). Ist eine CKD bereits vorbestehend („akut-auf-chronisch“), so ist die Prävalenz nochmals höher [34, 45]. Bei kritisch kranken Patient:innen auf der Intensivstation kann die Prävalenz für eine Hyperkaliämie bei > 50 % liegen [46].
Bei Patient:innen mit CKD variieren die in Studien dargelegten Prävalenzraten stark, was v. a. an den Komorbiditäten und der Medikation, aber auch an der Grunderkrankung liegt. Unter einer eGFR von 30 ml/min/1,73 m2 steigt die Hyperkaliämieprävalenz, bei einer weiteren Abnahme der eGFR, kontinuierlich an. Bei einer eGFR > 90 ml/min/1,73 m2 ist die Prävalenz < 1 %, diese erhöht sich bis zu einer eGFR < 15 ml/min/1,73 m2 (ohne Nierenersatztherapie [NET]) auf 35–50 % [34, 47].
Auch ältere Patient:innen haben ein höheres Risiko für eine Hyperkaliämie als jüngere: In einer Population von über 80-jährigen Patient:innen betrug die Prävalenz 16,9 %, verglichen mit nur 2,3 % in einer jungen Kohorte (16 bis 21 Jahre) [48].
Aktuell gibt es kaum Daten zum biologischen Geschlecht und Hyperkaliämie. Eine rezente Studie konnte jedoch eine signifikant höhere Prävalenz von Hyperkaliämien bei Männern mit CKD verglichen mit Frauen mit CKD finden [49]. Zu erwähnen ist hierbei aber, dass sich in dieser Studie Männer und Frauen in den Baseline-Charakteristika relevant hinsichtlich des Vorliegens von Diabetes mellitus, kardiovaskulären Erkrankungen, Verwendung von RAASi, Antihypertensiva und BMI unterschieden, diese Faktoren kamen allesamt deutlich häufiger bei Männern vor.
Im klinischen Alltag ist ein Zusammentreffen dieser Risikofaktoren ein häufiges Szenario. Eine CKD (hier definiert als eGFR < 60 ml/min/1,73 m2) besteht bei mehr als der Hälfte aller Patient:innen mit Herzinsuffizienz und/oder Diabetes. Diese Patient:innen erhalten häufig RAASi sowohl in Mono- als auch in Kombinationstherapien – und begünstigt durch interkurrente Erkrankungen treten dementsprechend häufig Hyperkaliämien auf [10].
Hyperkaliämie & Outcome
Eine Hyperkaliämie ist in verschiedenen Patient:innenpopulationen mit einer erhöhten Wahrscheinlichkeit für Hospitalisierung, intensivmedizinische Behandlung, kardiovaskuläre Ereignisse und Mortalität assoziiert [50]. Bei Notfallpatient:innen mit einer Hyperkaliämie relevanter Ausprägung (moderat bis schwer) sind die Hospitalisierungsrate und Mortalität klar erhöht [51, 52]. Um 2‑ bis 7‑fach höhere Mortalitätsraten werden bei Hyperkaliämien von vulnerablen Patient:innen mit CKD, DM, HF an der Intensivstation beobachtet [50, 53‐56].
Bei nicht-kritisch kranken Patient:innen mit CKD ≥ G3 ist das kurzfristige Risiko, bei Hyperkaliämien (5,5–6,0 bzw. > 6,0 mmol/l) zu versterben, geringer als bei Patient:innen ohne CKD [57]. Die Langzeitmortalität ist hingegen bereits ab [S‑K+] > 5,5 mmol/l erhöht [56, 58]. Bei Dialysepatient:innen ist die Mortalität erst mit einer Hyperkaliämie > 6,0 mmol/l um das 1,5- bis 2‑Fache höher und zusätzlich mit einer erhöhten Wahrscheinlichkeit für Hospitalisierung assoziiert [59‐61]. Des Weiteren wurden auch rezidivierende oder auch nur transiente Hyperkaliämieepisoden als Risikofaktor für Arrhythmien, kardiovaskuläre Ereignisse und einer erhöhten Sterblichkeit identifiziert [62‐64]. Jede weitere Komorbidität (CKD + DM + HF) steigert zudem das Mortalitätsrisiko additiv zum Schweregrad der Hyperkaliämie [54].
Physiologie des Kaliumhaushaltes – Regulation bei Kaliumbelastung
Kalium ist ein lebenswichtiger Mineralstoff und das wichtigste intrazelluläre Kation (98 % befinden sich im intrazellulären Raum [IZR], entsprechend einem Gesamtkörperkalium von 3000–3500 mmol). Es ist, reguliert durch die Na+-K+-ATPase, für die Aufrechterhaltung des zellulären Ruhemembranpotenzials verantwortlich. Mit einer üblichen „westlichen“ Ernährung werden täglich hohe Kaliummengen (60–120 mmol/Tag) über die Nahrung aufgenommen; diese Werte können aber je nach Art der Nahrung erheblich schwanken. Gesunde Nieren können diese großen Unterschiede der täglichen Kaliumzufuhr kompensieren. Auch andere physiologische Vorgänge sind für eine stabile Kaliumkonzentration im Blut und damit für die Funktion von Muskel- und Nervenzellen erforderlich.
Kalium ist Bestandteil von tierischen und pflanzlichen Nahrungsmitteln. Nach oraler Zufuhr wird das Elektrolyt innerhalb von 30–60 min über parazelluläre Wege passiv im Dünndarm resorbiert [65, 66]. Die Bioverfügbarkeit beträgt in Abhängigkeit von der Nahrungsquelle 60–90 %; Kalium tierischen Ursprungs wird deutlich besser resorbiert als aus pflanzlichen Quellen mit hohem Faseranteil (ca. 90 vs. 70 %) [67].
Nach der intestinalen Resorption wird Kalium sehr rasch in den IZR geshiftet, v. a. in die Muskulatur und Leber, um so einen zu raschen Anstieg der [S‑K+] zu verhindern. Diese postprandiale Reaktion wird über die Na+-K+-ATPase vermittelt, welche v. a. durch Insulin, aber auch durch Aldosteron und den aktuellen pH-Wert beeinflusst wird. Insbesondere die Zufuhr von Kohlehydraten gemeinsam mit Kalium, beispielsweise in Früchten, bewirkt durch die Insulinsekretion einen effektiven Kaliumshift [68]. Dadurch wird nur etwa die Hälfte der oral zugeführten Kaliummenge innerhalb von 3–6 h nach der Mahlzeit renal ausgeschieden und der Rest in den Zellen „abgepuffert“ [69, 70]. Bei körperlicher Aktivität können Katecholamine via Beta-2-adrenerge Rezeptoren und organische Anionen wie Laktat den Shift von Kalium in den IZR zusätzlich stimulieren [71].
Letztendlich muss aber der prandiale Kaliumüberschuss primär renal eliminiert werden (s. unten). Bereits bei der Nahrungszufuhr kann über einen noch nicht bekannten (intestinalen, hepatalen?) Faktor ein sog. Feed-forward-Mechanismus aktiviert werden [72]. Es setzt eine Kaliurese ein, noch bevor es zu einem Anstieg der [S‑K+] kommt, was auf Aldosteron-unabhängige Mechanismen hinweist (s. unten) [65]. Kalium wird frei glomerulär filtriert und anschließend im proximalen Tubulus bzw. im aufsteigenden Teil der Henle-Schleife unabhängig von der Nahrungszufuhr zu 90 % wieder rückresorbiert. Die renale Kaliumausscheidung findet folglich vorwiegend in den distalen Tubulusabschnitten statt. Hier erfolgt die Regulation der renalen Kaliumelimination in Abhängigkeit vom Natriumhaushalt (Volumenstatus). Bei Kaliumzufuhr und Euvolämie (kein erhöhtes Angiotensin II) wird die Natriumrückresorption am distalen Tubulus gehemmt, u. a. vermittelt durch „basolaterale Kaliumsensoren“, und in die Region des Sammelrohrs verschoben [73]. Dort erfolgt in der Akutphase, auch unabhängig von Aldosteron, die Natriumresorption durch den auf der luminalen Seite der Hauptzellen exprimierten epithelialen Natriumkanal (ENaC); dies liefert den elektrochemischen Gradienten, damit Kalium über die 2 wesentlichen Kaliumkanäle ROMK („renal outer medulla channel“) und BK („big kidney potassium channel“) sezerniert werden kann, ohne dass dabei zu viel Natrium verloren geht [74]. Während der ROMK konstitutionell aktiv ist, wird der BK bei Zunahme der tubulären Flussrate durch zirkumferenzielle Dehnreize zusätzlich aktiviert („flow-induced K+secretion“) [75]. Grundsätzlich ist aber ein gewisser Natriumanstrom an den distalen Tubulus erforderlich, damit Kalium im Austausch sezerniert werden kann – die Kaliumsekretion ist hier also eng an die Natriumresorption gekoppelt. Wird Kalium in Kombination mit Alkali zugeführt, kann es auch zusätzlich über die Zwischenzellen vom Typ B vermehrt ausgeschieden werden (Anmerkung: K‑Citrat wird besser ausgeschieden als KCl) (s. Abbildung Supplement 1) [76].
Binnen 30 min nach oraler Zufuhr von Kalium kann auch ein Anstieg von Aldosteron im Blut beobachtet werden. Kalium ist ein starker Stimulus für eine Aldosteronsekretion der Nebenniere, vermittelt durch Kaliumkanäle der Zona glomerulosa; ein Anstieg der [S‑K+] um 0,1 mmol/l erhöht die Aldosteronsekretion um 25 % [77]. Aufgrund seiner genomischen Wirkung ist aber der Effekt auf die Kaliumelimination erst einige Stunden später zu erwarten. Deshalb wird angenommen, dass Aldosteron v. a. für die Regulation der Kaliumelimination bei einer konstant hohen Zufuhr von Kalium verantwortlich ist [65]. Neben diesen Faktoren beeinflussen auch die Kaliumkonzentration im Serum, der Säure-Basen-Haushalt und die Vasopressinsekretion (stimuliert bei Hypovolämie den ROMK) die renale Kaliumelimination [78]. Eine weitere Auswirkung einer länger bestehenden Hyperkaliämie ist eine Reduktion der renalen Ammoniumausscheidung. Dies konnte sowohl im Tiermodell als auch am Menschen festgestellt werden und führt bei zusätzlicher Nierenfunktionseinschränkung zu einer metabolen Azidose (renal tubuläre Azidose [RTA] Typ IV) [79].
Ein verminderter Anstrom von Natrium im Sammelrohr (oft in Kombination mit der erhöhten Sekretion von Angiotensin II) verhindert, dass trotz hoher Aldosteronkonzentrationen Kalium renal verloren geht. Eine Hypovolämie kann also das Risiko für eine Hyperkaliämie deutlich erhöhen.
Zusammengefasst sind die Hauptmechanismen der renalen Kaliumsekretion die Natriumkonzentration im distalen Tubulus und die daraus resultierende Natriumreabsorption (via ENaC) im Aldosteron-sensitiven distalen Nephron – also auch die Aldosteronkonzentration – sowie die tubuläre Harnflussrate. Die maßgeblichen Organe der Kaliumhomöostase sind folglich Niere und Nebenniere.
Das Ausmaß der physiologischen intestinalen Kaliumelimination ist üblicherweise gering (10–15 mmol/Tag). Vor allem im Kolon kann, abhängig von der [S‑K+] und der Aldosteronkonzentration, Kalium aktiv sezerniert werden [80]. Bei anurischen Dialysepatient:innen kann dieser Weg der Kaliumelimination durchaus relevante Ausmaße annehmen, wie weiter unten ausgeführt ist.
Der Körper benötigt letztendlich in etwa 6–12 h, um die gesamte, oral zugeführte Menge an Kalium wieder zu eliminieren [81].
Symptome einer Hyperkaliämie
Die klinischen Manifestationen einer Hyperkaliämie betreffen Herz- und Skelettmuskulatur. Aufgrund der Gefahr des Herztods durch Arrhythmien ist eine schwere Hyperkaliämie ein medizinischer Notfall – nicht zuletzt gilt die Hyperkaliämie als eines der „4 H“ und somit als eine reversible Ursache eines Kreislaufstillstands. Allerdings erscheinen viele Patient:innen mit Hyperkaliämie klinisch asymptomatisch oder weisen nur subtile Symptome, wie beispielsweise allgemeine Schwäche, auf [4]. Eine Hyperkaliämie kann jedoch zu schwerer, typischerweise aszendierender Muskelschwäche führen, die letztlich auf den Stamm und die obere Extremität übergreifen kann [82‐84]. Die klinische Symptomatik einer Hyperkaliämie-assoziierten Myopathie wird mitunter mit jener eines Guillain-Barré-Syndroms verglichen [4].
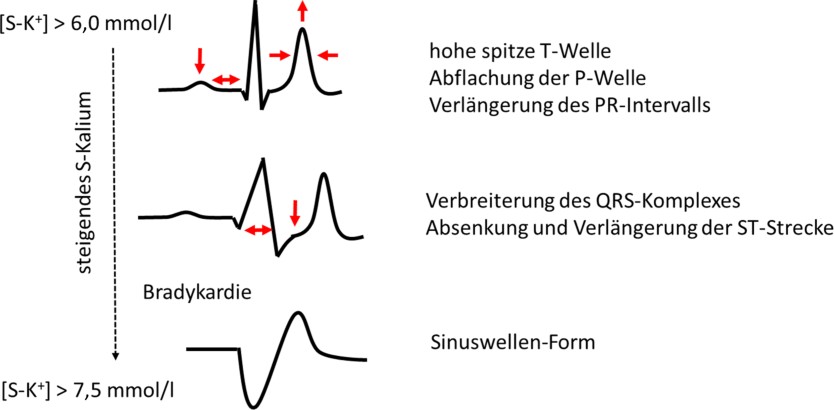
Die potenziell unmittelbar vital bedrohlichen Auswirkungen einer Hyperkaliämie sind jene auf das Myokard: Ein Anstieg der [S‑K+] führt initial zu einer Beschleunigung der kardialen Reizleitung durch ein Anheben des kardialen Ruhemembranpotenzials, d. h. es wird weniger negativ: −90 mV → −80 mV und nähert sich an das Schwellenpotenzial, was leichter Tachykardien verursachen kann. Weiters kommt es zu einer Beschleunigung der kardialen Repolarisation durch Aktivierung von Kaliumkanälen und damit zur Verkürzung des Aktionspotenzials [85]. Klassischerweise werden hohe T‑Wellen mit schmaler Basis als EKG-Veränderungen in der frühen Phase einer Hyperkaliämie beschrieben [86, 87]. Mit Zunahme der [S‑K+] kommt es hingegen durch ein weiteres Anheben des Ruhemembranpotenzials (> −75 mV) zu einer Inaktivierung der schnellen Natriumkanäle (Nav1.5) und damit zu einer Verzögerung des schnellen Einstroms von Natrium in der Phase 0 der Depolarisation [88]. Dadurch kann es zu einer Verlängerung des PR-Intervalls, einer Verbreiterung des QRS-Komplexes und einer Verkleinerung der Amplitude oder sogar einem Verlust der P‑Welle kommen [86, 89]. Schließlich kann es zum Auftreten einer Sinuswellenform im EKG und Bradykardien kommen ([86, 89]; s. Abb. 3). Obschon in der Literatur wiederholt ein typisches Muster von EKG-Veränderungen bei Hyperkaliämie in Abhängigkeit der Kaliumkonzentration angegeben wird, ist die diesbezügliche Studienlage überschaubar und teils widersprüchlich [90]. So konnten einige Studien zeigen, dass diese klassisch angegebenen Muster nicht verlässlich sind und Patient:innen mit relevanter Hyperkaliämie keine EKG-Veränderungen aufweisen müssen, bzw. die EKG-Veränderungen nicht zwangsläufig mit der [S‑K+] korrelieren [91, 92].
Kommentar
Insgesamt wird das EKG als ein unverlässlicher Parameter zur Detektion einer Hyperkaliämie angesehen, auch weil der Schweregrad der Hyperkaliämie nicht mit den EKG-Veränderungen korreliert [1, 93, 94]. Erste Studien zur künstliche Intelligenz-basierten EKG-Interpretation bezüglich Detektion einer Hyperkaliämie sind vielversprechend, zum aktuellen Zeitpunkt aber noch nicht in einem ausgereiften Stadium der klinischen Verlässlichkeit [95, 96].
Diagnostik der Hyperkaliämie
Messung der Kaliumkonzentration
Empfehlung
Die Blutabnahme sollte möglichst ohne Stauung erfolgen. Danach ist eine rasche Probenverarbeitung notwendig. Wird eine Hyperkaliämie festgestellt, so empfiehlt es sich, diese durch eine zweite Bestimmung, am besten durch eine venöse/arterielle Blutgasanalyse, zu bestätigen.
Kalium kann sowohl im Vollblut als auch im Serum bzw. Plasma gemessen werden. Bestimmungen im Serum ergeben typischerweise einen etwas höheren Kaliumwert (ca. +0,35 ± 0,3 mmol/l) als im Plasma [2, 3]. Aufgrund der raschen Verfügbarkeit der Analyse spielen Point-of-Care-Analysegeräte eine zentrale Rolle in der Diagnostik und im Management der Hyperkaliämie. Mitunter können aber klinisch relevante Unterschiede zwischen den Resultaten dieser Bestimmungsmethoden auftreten [97]. Insbesondere zur Kontrolle bei fraglich erhöhten Kaliumwerten kann die Analyse mittels Point-of-Care-Geräten eine wertvolle und rasche Hilfe darstellen [98]. Falsch erhöhte Kaliumwerte stellen in der klinischen Praxis ein häufiges Problem dar (s. Differenzialdiagnose der Hyperkaliämie-SCHRITT 2).
Bei einer [S‑K+] > 6,0 mmol/l steht primär die Therapie der Hyperkaliämie im Vordergrund (s. Abschnitt: Therapie der schweren Hyperkaliämie und Abb. 5). Eine Labordiagnostik zur Differenzialdiagnose sollte idealerweise parallel zur Therapie eingeleitet werden.
Erweiterte Labordiagnostik zur Abklärung der Ursachen einer Hyperkaliämie
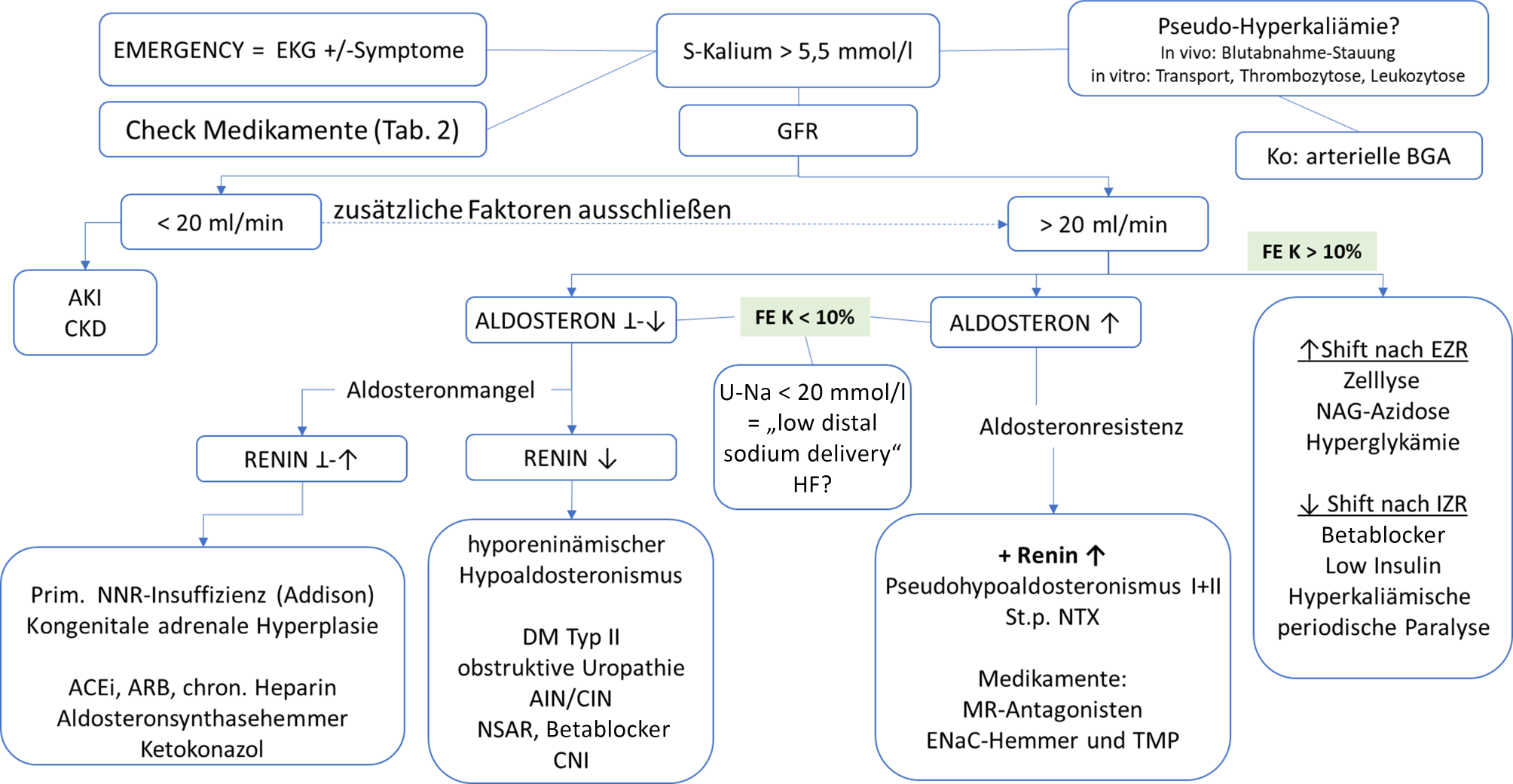
Für die Differenzialdiagnose werden die Anamnese (Risikofaktoren für eine Hyperkaliämie, Ernährung, Medikamente) und Klinik sowie eine erweiterte Labordiagnostik benötigt (Abb. 4: Differenzialdiagnose der Hyperkaliämie). Zuerst ist die Bestimmung der Nierenfunktion (Serum-Kreatinin, eGFR) erforderlich, in den meisten Fällen wird ein aktueller Kreatininwert bereits vorliegen [99]. Eine höhergradig eingeschränkte Nierenfunktion (akut oder chronisch) kann per se für eine Hyperkaliämie verantwortlich sein, das Risiko wird aber durch Kofaktoren entscheidend beeinflusst. Liegt die eGFR über 20–30 ml/min/1,73 m2, gewinnen andere bzw. zusätzliche Ursachen der Hyperkaliämie an Bedeutung – es sollte deshalb als Nächstes die renale Kaliumelimination beurteilt werden.
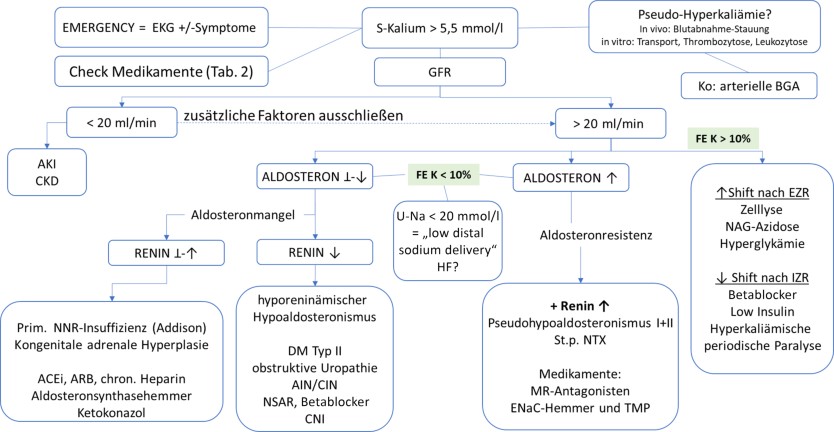
Der Goldstandard wäre die Messung der Kaliumausscheidung im 24-h-Harn. Dieser Test eignet sich naturgemäß nur für die Abklärung einer chronischen Hyperkaliämie. Gesunde Nieren können pro Tag 250–400 mmol Kalium ausscheiden, liegt ein Kaliummangel vor, kann die Ausfuhr auf 15–20 mmol/Tag reduziert werden [100]. Schneller, da aus dem Spontanharn berechenbar, ist die Bestimmung der fraktionellen Exkretionsrate von Kalium (FeK+) oder die Kalium-Kreatinin-Ratio im Harn, welche der Berechnung des transtubulären Kaliumgradienten in manchen Situationen überlegen ist [101] (Berechnung über: Nieren.app der ÖGN: Rechner). Aus einer täglichen Kaliumelimination von 250–400 mmol sollte – bei normaler GFR – rein rechnerisch die FeK+ > 40–50 % bzw. die K+-Kreatinin-Ratio > 20 mmol/mmol sein, wenn eine adäquate renale Kaliumelimination vorhanden ist [101]. Bei Hyperkaliämie weist eine FeK+ von > 15–20 % auf eine gute renale Kaliumelimination hin. Ist die FeK+ bei guter Nierenfunktion < 10 %, so ist von einer renalen Ursache der Hyperkaliämie auszugehen [102]. Mit Abfall der GFR steigt die FeK+ physiologisch an, sodass trotz höherer Werte der FeK+ eine inadäquate renale Kaliumelimination vorhanden sein könnte.
Ist die renale Kaliumexkretion gestört, so kann dies bei guter Nierenfunktion nur durch eine Beeinträchtigung des RAAS oder durch einen verminderten Anstrom von Natrium an den distalen Tubulus (Harn-Na+ < 20 mmol/l) verursacht sein. Da die diagnostische Wertigkeit der Harndiagnostik (24-h-Harnkalium oder FeK+) eingeschränkt sein kann, empfiehlt es sich, bei allen Patient:innen mit persistierender Hyperkaliämie das RAAS zu evaluieren: Es ist deshalb als Nächstes notwendig, Renin und Aldosteron im Serum zu bestimmen, wenn keine RAAS-Hemmer eingenommen werden (s. Tab. 1).
Wie erwähnt, ist eine Hyperkaliämie ein starker Stimulus für die Produktion von Aldosteron. Bereits bei [S‑K+] > 5,5 mmol/l ist eine Verdopplung der Plasma-Aldosteronkonzentration zu erwarten, steigt die [S‑K+] weiter an, kommt es zu einer Erhöhung um das 5‑ bis 10-Fache [103].
Bei einer [S‑K+] von > 5,5 mmol/l ist eine Aldosteronkonzentration < 9 ng/dl typisch für einen Aldosteronmangel, während ein Wert > 20 ng/dl (= adäquater Anstieg) auf eine Aldosteronresistenz hinweist [104]. Auch eine Aldosteron/Kalium-Ratio von < 2–3 kann als inadäquate Reaktion auf eine Hyperkaliämie bzw. Hinweis auf einen selektiven Aldosteronmangel herangezogen werden (Einheiten: Aldosteron [ng/dl]/Kalium [mmol/l]) [105]. Ist der Aldosteronmangel durch eine Unterfunktion der Nebenniere selbst bedingt (primäre Nebenniereninsuffizienz, Morbus Addison), verdoppelt sich die Reninkonzentration im Serum (ca. > 50–100 µIU/ml). Eine niedrige Renin- (< 5 µIU/ml) und Aldosteronkonzentration wird als hyporeninämischer Hypoaldosteronismus bezeichnet.
Kommentar
Die Referenzwerte für Aldosteron und Renin können zwischen unterschiedlichen Laborinstituten schwanken.
Aufgrund der Assoziation von metabolen Azidosen mit Hyperkaliämie wird bei jeder moderaten oder schweren Hyperkaliämie empfohlen, eine arterielle oder venöse Blutgasanalyse durchzuführen.
Differenzialdiagnose der Hyperkaliämie – Algorithmus und dessen Erklärung
Die Differenzialdiagnose erfolgt anhand eines Algorithmus (Abb. 4).
SCHRITT 1: Besteht eine Notfallsituation (symptomatische Hyperkaliämie)?
Wenn ja, s. Abb. 5.
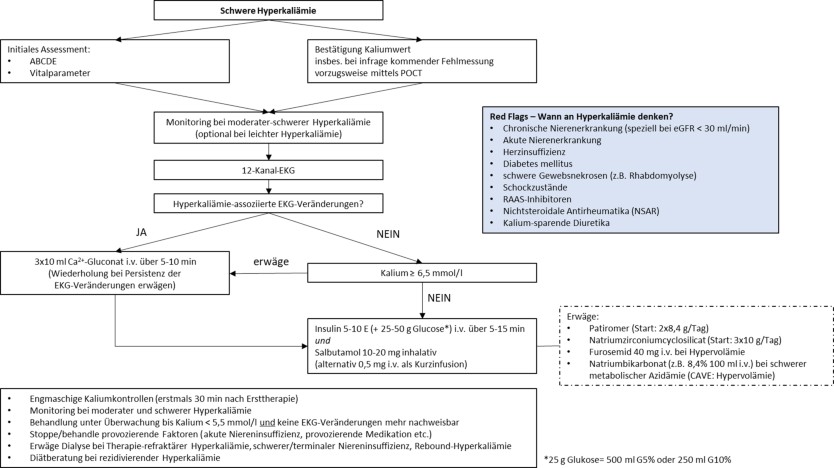
Abb. 5 Therapie der schweren Hyperkaliämie
SCHRITT 2: Ausschluss einer Pseudohyperkaliämie
Als Pseudohyperkaliämie bezeichnet man eine artifizielle Erhöhung der [S‑K+]. Es kommt dabei zu keiner klinischen Symptomatik oder EKG-Veränderungen. Die häufigste Ursache ist eine Hämolyse bei der Blutabnahme (langes Stauen, heftiges Pumpen mit der Hand, starke Sogwirkung bei Blutabnahme), welche von einer Erhöhung der LDH begleitet wird und im Labor durch Bestimmung des freien Hämoglobins nachgewiesen werden kann (H-Index = Hämolysegrad in der Probe) [106]. Es kann aber auch zu einer Ex-vivo-Freisetzung von Kalium bei Thrombozytose oder Leukozytose im Rahmen von myelo- oder lymphoproliferativen Erkrankungen oder bei langem Transport von gekühlten Proben kommen [107‐110]. Die irrtümliche Verwendung von K+-EDTA-beschichteten Blutröhrchen oder die Blutabnahme bei laufender Infusion einer kaliumhaltigen Lösung erhöht ebenfalls die Kaliumkonzentration [111]. Sehr selten sind die familiären Formen der Pseudohyperkaliämie, bei denen es bei niedrigen Temperaturen (< 20 °C) in vitro durch Mutation am ABCB6 oder SLC4A1 zu einer Freisetzung von Kalium aus den Erythrozyten kommt [112]. Im Zweifelsfall sollte eine Hyperkaliämie durch eine Blutgasanalyse bestätigt werden. Müssen Blutproben versendet werden, dann sollten diese vorher zentrifugiert werden.
Es gibt auch tageszeitliche Schwankungen der [S‑K+]. Nachts sind die Konzentrationen um ca. 0,3–0,4 mmol/l niedriger als unter Tag, aber immer im Normbereich gelegen [113, 114]. Auch nach einer sehr kaliumreichen Kost kann die [S‑K+] um bis zu 0,5 mmol/l ansteigen [70]. Bis auf wenige Ausnahmen, z. B. bei Dialysepatient:innen, macht es keinen signifikanten Unterschied, ob die Blutabnahme nüchtern oder nicht nüchtern erfolgt. Bei Patient:innen mit CKD können auch erhebliche Unterschiede zwischen prä- und den höheren postprandialen Kaliumwerten bestehen [115].
SCHRITT 3: Wie ist die Nierenfunktion?
eGFR < 20–30 ml/min/1,73 m2: Eine hochgradig reduzierte exkretorische Nierenfunktion (akut oder chronisch) kann eine Hyperkaliämie per se erklären. In vielen Fällen sind aber zusätzliche Faktoren relevant. In der Praxis sollte deshalb auch bei diesen Patient:innen an andere Ursache für eine Hyperkaliämie gedacht werden (s. Abb. 4), z. B. neu eingeleitete Therapie mit RAASi, kaliumreiche Kost, Kaliumshift, Zelllyse etc.
eGFR > 20–30 ml/min/1,73 m2: Eine normale oder nicht hochgradig eingeschränkte Nierenfunktion sollte die [S‑K+] stabil halten können. Für die DD s. SCHRITT 4.
SCHRITT 4: Wie ist die renale Kaliumelimination?
FeK+ > 10 %: Die renale Kaliumelimination ist adäquat. Es kann aber durch Shiftbewegungen zwischen extrazellulärem Raum (EZR) und IZR die [S‑K+] erhöht sein.
Vermehrter Ausstrom von Kalium aus der Zelle in den EZR: Ein Zellzerfall bei Tumorlysesyndrom oder eine Rhabdomyolyse können schwere Hyperkaliämien verursachen. Diese Diagnosen ergeben sich aber üblicherweise aus dem klinischen Kontext. Auch eine Azidämie kann zu einem Shift von K+ im Austausch mit H+ aus der Zelle führen: Dabei sind metabole Azidosen mit normaler Anionenlücke im Gegensatz zu Formen mit hoher Anionenlücke oder respiratorische Azidosen viel häufiger von einer Hyperkaliämie begleitet [116]. Einzige Ausnahme ist die distale RTA (Typ 1), welche zu einer Hypokaliämie führt [79, 117]. Auch Zustände mit hoher Plasmatonizität (schwere Hyperglykämie – v. a. mit Ketoazidose, oder nach der Verabreichung von großen Mengen an Kontrastmittel) führen durch einen Shift von Wasser in den EZR zu einer Erhöhung der [K+] im IZR und in Folge zum Shift von Kalium in den EZR („solvent drag“) [118].
Verminderte Aufnahme von Kalium in die Zelle: Betablocker oder eine zu niedrige Insulinkonzentration hemmen den postprandialen Kaliumtransport in die Zelle. Auch die hyperkaliämische periodische Paralyse ist durch eine Störung des Natrium-vermittelten Kaliumtransports (SCN4A) in die Muskelzelle charakterisiert. Hyperkaliämien sind getriggert durch Kälte, Hunger und Kaliumzufuhr bzw. nach körperlicher Anstrengung [119].
FeK+ < 10 %: Die renale Kaliumelimination ist gestört – weiter mit SCHRITT 5.
SCHRITT 5: Messung von Renin und Aldosteron (wenn keine RAASi eingenommen werden)
Bei gering eingeschränkter Nierenfunktion ist ein Hypoaldosteronismus die wichtigste Ursache für eine Hyperkaliämie mit verminderter renaler Kaliumelimination. Wir unterscheiden eine Aldosteronresistenz von einem Aldosteronmangel (s. Diagnostik und Abb. 4). Beide Formen sind mit einer metabolen Azidose assoziiert und werden entsprechend auch als RTA Typ IV bezeichnet [120]. Durch die Interpretation von Renin und Aldosteron bzw. der Messung des systemischen Blutdrucks erfolgt die weitere Differenzialdiagnose:
1.
- Aldosteronresistenz (Renin ↑, Aldosteron ↑): An erster Stelle in der DD gilt es, medikamentöse Ursachen auszuschließen: MRA, kaliumsparende Diuretika, aber auch Trimethoprim hemmen die Wirkung von Aldosteron durch die Blockade des MR bzw. des ENaC. An zweiter Stelle ist an tubulointerstitielle Nierenerkrankungen zu denken.
Viel seltener sind angeborene Loss-of-Function-Mutationen des ENaC oder MR (Pseudohypoaldosteronismus Typ Ia/Ib): Diese Erkrankungen sind charakterisiert durch renalen Salzverlust (Hypotonie), Hyponatriämie und Hyperkaliämie [121]. Ähnliche Zustände können auch (v. a. bei Kindern) bei obstruktiver Uropathie beobachtet werden [122].
Wichtig ist es in dieser Situation, auch noch auszuschließen, dass ein geringer Anstrom von Na+ an das Sammelrohr die Kaliumsekretion hemmt ([Harn-Na+] < 20 mmol/l). Dieser Mechanismus kann bei Hypovolämie oder kardialer Dekompensation die Ursache für eine Hyperkaliämie sein. Ein anschauliches Beispiel stellt das BRASH-Syndrom dar (Bradykardie, Renal Failure, AV‑Block, Schock und Hyperkaliämie). Beim BRASH-Syndrom können auch [S‑K+] < 6,0 mmol/l zu relevanten EKG-Veränderungen führen [123]. - Aldosteronmangel: Dieser kann entweder durch eine direkte Störung der Aldosteronproduktion der Nebenniere (Renin ↑, Aldosteron ⊥–↓), oder indirekt durch eine verminderte Reninproduktion (Renin ↓, Aldosteron ⊥–↓) bedingt sein.
- a) Direkte Störung der Aldosteronproduktion (Renin ↑, Aldosteron ⊥–↓)
- aa) Primäre Nebennierenrindeninsuffizienz:
Bei dieser Form des Hypoaldosteronismus muss immer ein begleitender Hypocortisolismus ausgeschlossen werden, da dieser wesentlich häufiger anzutreffen ist als der isolierte Hypoaldosteronismus.
Erworbene Ursachen für eine verminderte Aldosteronproduktion im Rahmen einer primären Nebennierenrindeninsuffizienz sind die Autoimmunadrenalitis oder Metastasen/Tuberkulose der Nebennieren, welche auch Ursache für eine Addison-Krise sein können. Da bei sekundärer Nebenniereninsuffizienz (also bei zugrunde liegender hypophysärer Pathologie mit ACTH-Mangel) die Zona glomerulosa, also der Ort der Aldosteronproduktion, intakt ist (und Aldosteron v. a. über die Renin-Angiotensin-Achse stimuliert wird), findet sich hier üblicherweise keine Hyperkaliämie.
Auch bei einigen Formen der kongenitalen adrenalen Hyperplasie, welche mit einem Mangel an Mineralokortikoiden (Mutationen am CYP21A2, HSD3B2 oder CYP11B2) einhergehen, können Hyperkaliämien beobachtet werden [124]. - ab) Isolierter Hypoaldosteronismus:
Der klassische isolierte Hypoaldosteronismus (mit Renin ↑) ist gekennzeichnet durch eine Hypovolämie [125]. Dieser hyperreninämische Hypoaldosteronismus kann manchmal bei kritisch kranken Patient:innen beobachtet werden [126].
Häufiger sind Zustände, bei denen Medikamente die Aldosteronproduktion hemmen. ACEi hemmen die Bildung von ATII, während ARB direkt die Wirkung von ATII an der Nebenniere hemmen. Beide unterdrücken die ATII (und damit v. a. die durch eine Hypovolämie) induzierte Bildung von Aldosteron. Heparin reduziert hingegen die Expression von ATII-Rezeptoren an der Nebenniere [127]. Die Aldosteronsynthese wird direkt durch Aldosteronsynthasehemmer, wie z. B. Lorundrostat, gehemmt [128].
- aa) Primäre Nebennierenrindeninsuffizienz:
- b) Indirekte Störung der Aldosteronproduktion (Renin↓, Aldosteron Ʇ–↓)
- ba) Hyporeninämischer Hypoaldosteronismus: mit normalem oder erhöhtem Blutdruck
In dieser Situation ist die Cortisolproduktion nicht verändert.
Medikamente: NSAR, Renininhibitoren und Betablocker können durch Hemmung der Reninbildung sekundär zu einem Hypoaldosteronismus führen.
Bei Menschen mit Diabetes kann häufig eine inadäquat niedrige Stimulation der Reninbildung beobachtet werden [129]. Daneben sind auch andere Faktoren bei Diabetes relevant für die reduzierte renale Kaliumelimination. Ein Hyperinsulinismus stimuliert die Na+-Resorption am proximalen und distalen Tubulus und stört damit die Na+-Anflutung ans Sammelrohr [130]. - bb) Pseudohypoaldosteronismus Typ II (Gordon-Syndrom):
Durch eine Gain-of-Function-Mutation kommt es zu einer Stimulierung des Na+-Transportes am distalen Tubulus, was die Na+-abhängige Kaliumsekretion am Sammelrohr stört; die Folge ist neben einer Hyperkaliämie eine Hypertonie. Auch in dieser Situation sind Renin und Aldosteron durch die Hypervolämie supprimiert [131, 132]. Die Einnahme von Calcineurininhibitoren (Cyclosporin A, Tacrolimus) hat einen ähnlichen stimulierenden Effekt auf den NaCl-Kotransporter am distalen Tubulus, beeinflusst aber auch über andere Mechanismen die renale Kaliumsekretion [133, 134]. Neben der Immunsuppression bestehen bei Patient:innen nach einer Nierentransplantation mehrere Faktoren (Komorbiditäten, Medikamente), welche das Risiko für eine Hyperkaliämie erhöhen [135, 136].
- ba) Hyporeninämischer Hypoaldosteronismus: mit normalem oder erhöhtem Blutdruck
- a) Direkte Störung der Aldosteronproduktion (Renin ↑, Aldosteron ⊥–↓)
Risikofaktoren für eine Hyperkaliämie
Basierend auf der Physiologie der Kaliumhomöostase können typische Risikofaktoren für die Entwicklung einer Hyperkaliämie definiert werden [137]. Wie eingangs erwähnt, liegen in der Praxis jedoch oftmals mehrere dieser Risikofaktoren gleichzeitig vor [54].
Nierenfunktion
Die Nieren sind das Schlüsselorgan für die Kaliumausscheidung. Bei CKD adaptieren sich die noch funktionierenden Nephrone und erhöhen den Anteil der tubulären Kaliumsekretion und damit die Kaliumelimination, sodass erst ab einer eGFR < 30 ml/min/1,73 m2 das Risiko für eine Hyperkaliämie ([S‑K+] > 5,5 mmol/l) deutlich ansteigt [138]. Bei AKI sind diese adaptiven Mechanismen noch nicht aktiv, was die Wahrscheinlichkeit für Hyperkaliämien deutlich erhöht [45, 139].
Bei Patient:innen an der Hämodialyse sind moderat erhöhte prädialytische Kaliumwerte bei ca. 50–70 %, schwere Hyperkaliämien bei 17 % anzutreffen [81, 140]. Das Risiko für eine prädialytische Hyperkaliämie ist nach dem langen dialysefreien Intervall (Sa → Di oder Fr → Mo) mehr als doppelt so hoch wie vor den anderen Dialysetagen und erhöht das Risiko eines plötzlichen Herztodes [141, 142]. Speziell bei Dialysepatient:innen kann auch eine Nüchternhyperkaliämie beobachtet werden. Ursache dafür ist ein Shift von K+ aus dem IZR durch einen niedrigen Insulinspiegel, welcher renal nicht kompensiert werden kann [143]. Dies kann beispielsweise präoperativ von Relevanz sein, wenn Patient:innen über Nacht nüchtern bleiben und am Folgetag eine Hyperkaliämie aufweisen. Die Kaliumelimination über das Kolon (via BK-Kanäle) ist bei terminaler Nierenerkrankung von Bedeutung, weil sie im Vergleich zu nierengesunden Menschen von 10–20 mmol/Tag auf ca. 40–75 mmol/Tag gesteigert sein kann [66, 144]. Während ACEi und ARB das Risiko für Hyperkaliämien bei NET nicht relevant erhöhen, konnte dies bei Betablocker, Digoxin und Heparin beobachtet werden [145]. In der rezenten ACHIEVE-Studie wurde aber ein um 50 % höheres Risiko für schwere Hyperkaliämien unter dem MRA Spironolacton in der Dosis von 25 mg/Tag beobachtet, Ähnliches gilt auch für Eplerenon bei Dialyse [146, 147]. Insulin, Salbutamol, Hyperglykämie und Azidose beeinflussen an der NET den K+-Shift ähnlich wie bei normaler Nierenfunktion. Auch nach stärkerer körperlicher Anstrengung (Rhabdomyolyse), Rückgang der Restnierenfunktion, Problemen mit dem Dialysezugang oder längeren Phasen von Obstipation werden Hyperkaliämien beobachtet [81, 148].
Peritonealdialysepatient:innen haben ein etwas geringeres Risiko für eine Hyperkaliämie, was auf die kontinuierliche Dialyse mit einem kaliumfreien Dialysat und eine initial bessere Restnierenfunktion inklusive einer üblicherweise breiteren Anwendung von Schleifendiuretika zurückzuführen ist. Dies begünstigt aber auch die Neigung zu Hypokaliämien (10–36 % der Patient:innen). Mit Rückgang der Restnierenfunktion steigt aber das Risiko für Hyperkaliämien auch bei Peritonealdialysepatient:innen wieder an [145].
Medikamente, welche die renale Kaliumelimination beeinflussen
Medikamente, welche die renale Kaliumelimination beeinflussen, sind in Tab. 1 abgebildet.
Am bedeutendsten sind Hemmer des RAAS, da sie die renale Kaliumelimination stören [149]. Der Eingriff in das RAAS kann an verschiedenen Stellen erfolgen: Hemmung der Reninfreisetzung, ACEi, ARB, Störung der Aldosteronsynthese, MRA, Hemmer des ENaC [87]. Die Relevanz von ACEi, ARB, MRA, Renininhibitoren und ASI, welche die Aldosteron-abhängige renale Kaliumelimination beeinflussen, ist im Abschnitt Epidemiologie und in Abb. 2 beschrieben, welche auch auf die Interaktion zwischen Medikation und Komorbiditäten eingeht. Kaliumsparende Diuretika wie Amilorid erhöhen die [S‑K+] etwas weniger stark als Spironolacton [150]. Nicht zu vergessen ist auch eine dosisabhängige Risikoerhöhung bei Verwendung von MRA (Hyperkaliämieprävalenz bei 25 mg Spironolacton 13,5 %, bei 50 mg Spironolacton 41 % – RALES) oder kaliumsparenden Diuretika [26, 150]. Trimethoprim ist ein kompetitiver Inhibitor des ENaC (ähnlich wie Amilorid) und kann v. a. bei älteren Patient:innen mit CKD innerhalb von wenigen Tagen die [S‑K+] um bis zu 1,2 mmol/l erhöhen [151].
NSAR hemmen die Prostaglandin-vermittelte Freisetzung von Renin und Aldosteron, v. a. bei Hypovolämie, und erhöhen damit das Risiko einer Hyperkaliämie [152]. Während das Risiko für Hyperkaliämien bei der Einnahme von NSAR bei älteren Menschen ohne Risikofaktoren insgesamt sehr gering ist (< 1 %), steigt die Prävalenz in der Risikopopulation deutlich (bis ca. 15 %) [153, 154]. Vor allem bei einer begleitenden Hypovolämie oder unter RAASi wirkt sich der Effekt von NSAR auf die Kaliumelimination am deutlichsten aus [152, 155]. Auch nichtselektive Betablocker (Hemmung der Reninbildung) oder Calcineurininhibitoren beeinflussen das RAAS und damit die renale Kaliumelimination [29, 156].
Kommentar
- Viele prospektiven Studien zur Therapie mit RAASi inkludierten ausschließlich Patient:innen mit [S‑K+] von maximal 4,8 mmol/l vor Therapiebeginn oder mit niedrigem Risikoprofil, z. B. Hypertonie ohne CKD, sodass bei breiter Anwendung in „real life“ höhere Raten an Hyperkaliämien zu erwarten sind, wie es bereits nach der Publikation der RALES-Studie zu beobachten war [157]. Obwohl die meisten Hyperkaliämien unter RAASi bereits wenige Wochen nach dem Therapiebeginn auftreten, beeinflusst auch die unterschiedliche Studiendauer die Zahlen zur Prävalenz der Hyperkaliämie.
- Im Prinzip sind Substanzen, welche das RAAS hemmen, bei stabilen Patient:innen relativ sichere Medikamente in Bezug auf das Risiko, eine Hyperkaliämie zu entwickeln. Die meisten Episoden treten dann auf, wenn ein aktives RAAS benötigt wird (z. B. bei Hypovolämie-AKI), weshalb die Einhaltung der „sick day rules“ essenziell ist. In dieser Situation gilt es zu beachten, dass manche RAASi wie Spironolacton eine deutlich längere Wirkdauer haben als andere, wie z. B. Eplerenon und Finerenon.
- Jede Dosiserhöhung eines RAASi, jeder Neubeginn einer Medikation, welche das RAAS beeinflussen kann (z. B. NSAR), und jede Aggravierung einer Komorbidität erhöhen das Hyperkaliämierisiko und erfordern deshalb eine zeitnahe Kontrolle der [S‑K+].
Komorbiditäten Herzinsuffizienz, Diabetes und Hypertonie
Bei HF sind sowohl die Phasen der Dekompensation als auch jene der Hypovolämie relevant; durch die vermehrte Natriumretention am weiter proximal gelegenen Tubulusapparat reduziert sich der Na+-Anstrom an den distalen Tubulus und verhindert dadurch – trotz hoher Aldosteronaktivität – eine suffiziente Kaliumelimination. Weiters werden Patient:innen mit HF fast immer mit RAASi behandelt [10, 158].
Menschen mit Diabetes haben neben einer CKD oft auch unabhängig von einer RAASi-Therapie Zeichen eines hyporeninämischen Hypoaldosteronismus [159]. Auch ein nicht optimal therapierter Diabetes kann durch die Aktivierung des Shifts von Kalium in den EZR bei Hyperglykämie eine Hyperkaliämie begünstigen.
Eine therapierefraktäre Hypertonie ist eine der Hauptgründe für eine Intensivierung der RAASi, v. a. durch Einleitung einer Therapie mit einem MRA. Diese Wirkstoffgruppe hat bei Abwesenheit anderer Komorbiditäten ein geringeres Risiko für eine Hyperkaliämie, was zum Teil auch auf einen begleitenden Hyperaldosteronismus zurückzuführen sein könnte (2 % in der PATHWAY-2-Studie) [35].
Kaliumzufuhr
Wie weiter oben dargelegt, ist die Kaliumeliminationskapazität der gesunden Niere sehr hoch. Nur in Kombination mit anderen Risikofaktoren (CKD, Medikamente) kann eine hohe Kaliumzufuhr zu einer Hyperkaliämie führen. Bei Patient:innen mit weit fortgeschrittener CKD ist die basale Kaliumsekretion maximiert und kann nach einer oralen Kaliumbelastung nicht weiter stimuliert werden. Daher kann es zu einem relevanten postprandialen Anstieg der [S‑K+] kommen (0,4–1,0 mmol/l), der bis zu 6 h nach der Mahlzeit anhält [1, 115, 143, 160, 161]. Wird das Kalium in Alkali-Form und in Früchten mit hohem Faseranteil zugeführt, so reduziert sich das Risiko einer postprandialen Hyperkaliämie, weshalb Diätvorschriften für Dialysepatient:innen zuletzt etwas gelockert wurden bzw. differenzierter betrachtet werden [115]. Vorsicht ist auch bei Risikopatient:innen gegeben, wenn Kaliumsupplemente verordnet werden (inklusive Diätsalz-KCl).
Die innerhalb von 24 Stunden ausgeschiedene Kaliummenge im Harn eignet sich selbst bei normaler Nierenfunktion nur eingeschränkt zur Beurteilung der täglichen Kaliumzufuhr und verliert bei CKD oder unter Beeinflussung des RAAS vollständig ihre Aussagekraft [149, 162]. Die Erhebung der Kaliumzufuhr erfolgt durch die Ernährungsberatung anhand von Aufzeichnungen der konsumierten Nahrungsmittel über zumindest 3 Tage.
Frühere Episoden einer Hyperkaliämie
Patient:innen, welche schon einmal eine Episode einer Hyperkaliämie erlitten haben, haben ein deutlich erhöhtes Risiko für weitere Episoden; je öfter die Hyperkaliämie aufgetreten ist, umso wahrscheinlicher ist eine neuerliche Episode und umso höher ist auch die Mortalität [29, 163, 164].
Alter
Im Alter steigt das Risiko für Hyperkaliämien. Dies beruht nicht nur auf einer Abnahme der GFR und einer reduzierten Reninsekretion, sondern auch auf einer verminderten Aldosteronproduktion nach Kaliumzufuhr [165]. Weitere Risikofaktoren für Hyperkaliämie, speziell bei älteren Patient:innen, sind ein niedriger BMI und Gebrechlichkeit; beides ist assoziiert mit einer niedrigeren Muskelmasse, was die Kapazität, Kalium aufzunehmen, reduziert [166].
Protektive Faktoren
Dem allen stehen gewisse protektive Faktoren gegenüber: Medikamente wie Schleifendiuretika, Thiaziddiuretika und SGLT2-Hemmer können das Risiko für eine Hyperkaliämie in verschiedenen Situationen (RAASi, CKD, DM) reduzieren [29, 167].
Risikokalkulatoren
Optimal wäre es, das Risiko für die Entwicklung einer Hyperkaliämie z. B. vor dem Beginn einer RAASi-Therapie zu evaluieren, um entsprechende Kontrollintervalle zur Messung der [S‑K+] definieren zu können. Ein möglicher Risikoscore wurde anhand der FIDELITY-Studie (CKD + DM) evaluiert. Die Risikofaktoren eGFR < 45 ml/min/1,73 m2, Albumin/Kreatinin-Ratio im Harn (UACR) > 1 g/g, [S‑K+] > 4,5 mmol/l, Anamnese einer früheren Hyperkaliämieepisode, Hb < 12 g/dl, keine Thiaziddiuretika oder SGLT2‑Hemmer in der adjuvanten Therapie beeinflussten das Hyperkaliämierisiko signifikant [168]. Der SCREAM-Score hilft, das Hyperkaliämierisiko basierend auf ähnlichen Faktoren (zusätzlich DM) bei Einleitung einer ACEi oder ARB-Therapie abzuschätzen [11]. Bei Patient:innen mit CKD existiert ebenfalls ein Risikokalkulator für die Hyperkaliämie (Faktoren: ACEi, Azidose, DM, HF, frühere Hyperkaliämie, CKD-Stadium, Alter > 75 a) [169].
Management der schweren Hyperkaliämie
Oft werden die Begriffe akute und schwere Hyperkaliämie synonym verwendet, was nachvollziehbar ist, da diese häufig gleichzeitig auftreten. Da sich die Therapie der Hyperkaliämie am Schweregrad orientiert, wird hier der Begriff schwere Hyperkaliämie bevorzugt verwendet. Eine sich schnell entwickelnde, schwere Hyperkaliämie ist aber (auch aufgrund der auslösenden Ursache) meistens bedrohlicher als eine langsam entstehende, was sich aus den Mortalitätsdaten bei chronisch nierenkranken Menschen ableiten lässt [57].
Grundsätzlich gilt: Eine akute Störung ist bedrohlicher als eine chronische!
Bislang gibt es nur wenige hochqualitative Studien zum Management der Hyperkaliämie. Eine 2018 abgehaltene „Controversies Conference“ der KDIGO und 2 daraus resultierende Publikationen erarbeiteten Expertenempfehlungen auf Basis der vorhandenen Evidenz [1, 4]. Im Folgenden wird auf diesen Empfehlungen aufgebaut und um seither publizierte Studien ergänzt.
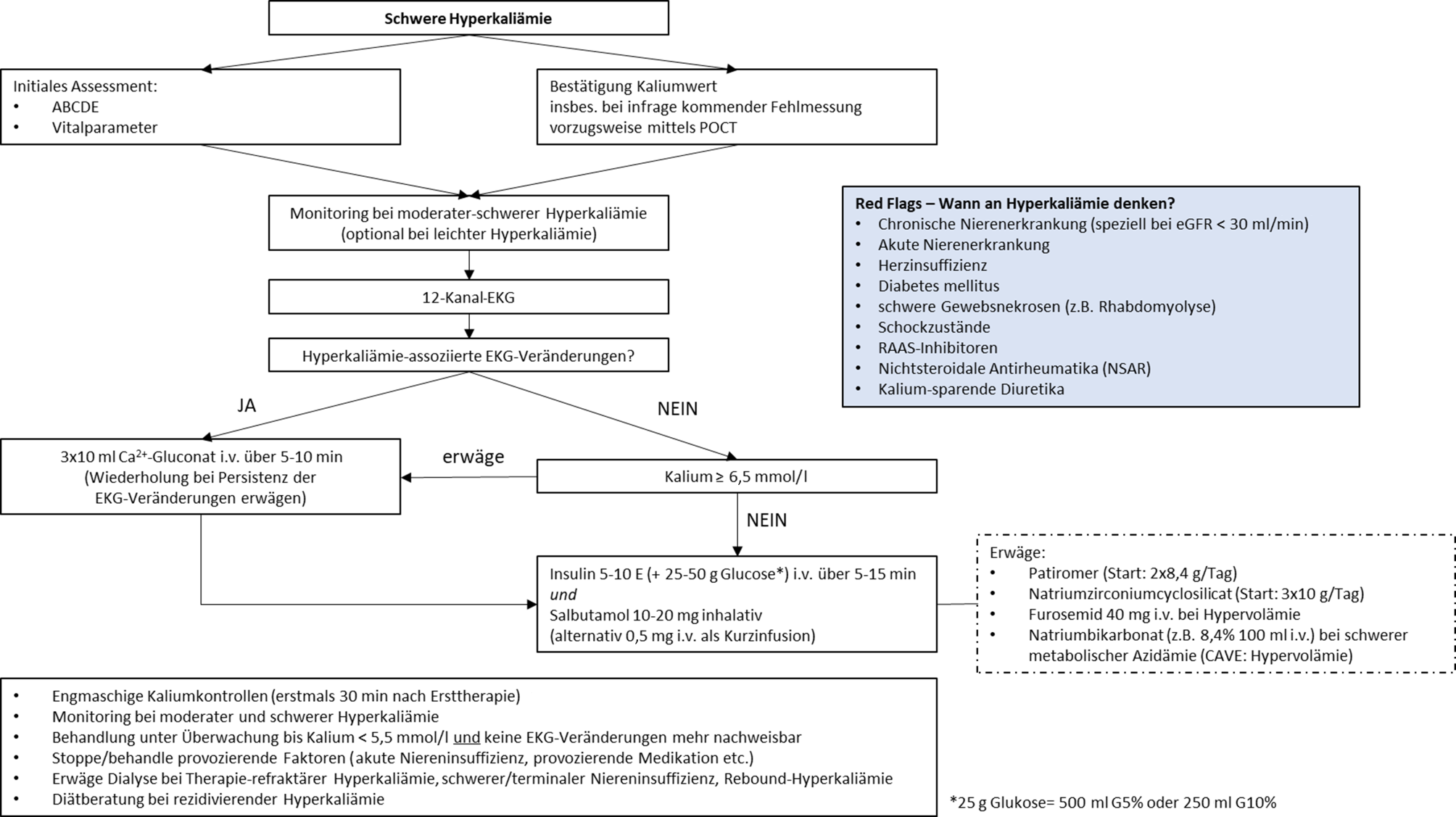
Basismanagement der schweren Hyperkaliämie
Bei Verdacht auf das Vorliegen einer schweren Hyperkaliämie empfehlen wir eine zügige Ersteinschätzung durch Messung der Vitalparameter, einer fokussierten Anamnese inklusive sorgfältiger Medikamentenanamnese und körperlicher Untersuchung, um eine akute vitale Bedrohung auszuschließen [4]. Klinische Erscheinungen sind zumeist erst bei [S‑K+] > 6,0 mmol/l zu erwarten. Die A (Airway), B (Breathing), C (Circulation), D (Disability), E (Exposure)-Herangehensweise erscheint dabei eine effiziente Methodik darzustellen [170]. Red Flags, die an das Vorliegen einer schweren Hyperkaliämie denken lassen sollen, sind wie folgt [4]:
- CKD (speziell bei eGFR < 30 ml/min/1,73 m2),
- akute Nierenerkrankung,
- Herzinsuffizienz,
- Diabetes mellitus,
- schwere Gewebsnekrosen (z. B. Rhabdomyolyse),
- Schockzustände,
- RAASi, NSAR, kaliumsparende Diuretika (s. Abb. 5).
Eine zügige Bestimmung der [K+] ist anzustreben, wobei hierfür eine Analyse des Kaliums aus Vollblut mittels Point-of-Care-Geräten aufgrund des rasch verfügbaren Ergebnisses zu präferieren ist. Die Bestätigung einer Hyperkaliämie durch Bestimmung der [S‑K+] im Zentrallabor oder durch eine Blutgasanalyse ist anzustreben. Im klinischen Alltag wird selbst eine schwere Hyperkaliämie häufig im Rahmen einer routinemäßigen Blutabnahme als Zufallsbefund zum Aufnahmezeitpunkt diagnostiziert.
Die Anfertigung eines 12-Kanal-EKGs ist so rasch wie möglich in jedem Fall einer [S‑K+] > 6,0 mmol/l indiziert. Finden sich EKG-Veränderungen, so muss sofort eine Therapie eingeleitet werden. Die Etablierung einer Überwachung mit kontinuierlichem EKG-Monitoring, nicht-invasive Intervallmessung des Blutdruckes sowie Messung der Sauerstoffsättigung sind bei allen Patient:innen mit moderater bis schwerer Hyperkaliämie (s. Abb. 1 und 5) in der Notaufnahme indiziert. Besondere Beachtung ist der Tatsache zu schenken, dass auch sehr hohe [S‑K+] (> 7,0 mmol/l) mitunter nicht in (typischen) EKG-Veränderungen resultieren müssen (s. Symptome) [86, 93, 94, 171]. Patient:innen mit EKG-Veränderungen haben ein erhöhtes Risiko für das kurzfristige Auftreten eines kardiovaskulären Ereignisses [172].
Therapie einer schweren Hyperkaliämie
Die medikamentöse Therapie einer schweren Hyperkaliämie kann in 3 Säulen eingeteilt werden, wobei den ersten beiden initial die größte Bedeutung zukommt:
1. Antagonisierung der Kaliumwirkung auf die Erregungsleitung des Herzens bei EKG-Veränderungen,
2. Kalium-Shift von extra- nach intrazellulär,
3. Kaliumelimination (Niere, Darm).
Alle Maßnahmen können und sollen so rasch wie möglich und parallel zueinander initiiert werden, da sich dies positiv auf die Mortalität auswirken kann [173].
Weitere Maßnahmen zur Therapie der schweren Hyperkaliämie:
4. Therapie von Risikofaktoren
5. Nierenersatztherapie
6. Monitoring
1. Therapie von Arrhythmien mittels Kalziumsalzen
Bei Patient:innen mit moderater bis schwerer Hyperkaliämie und lebensbedrohlichen-EKG-Veränderungen (Verlust von P‑Wellen, verbreiterter QRS-Komplex, Sinuswellenform, Bradykardie) empfehlen wir die Verabreichung von Kalziumsalzen, präferenziell Calciumgluconat 3‑mal 10 ml 10 % i.v. über einen Zeitraum von 5–10 min. Bei Persistenz der EKG-Veränderungen 5 min nach der Verabreichung kann eine wiederholte Gabe in Betracht gezogen werden [4, 156]. Die Verabreichung soll zeitgleich von anderen Maßnahmen zur Kaliumsenkung begleitet werden.
Die Verabreichung von Kalziumsalzen ist in aktuellen Behandlungsrichtlinien wie den Guidelines des European Resuscitation Councils (ERC), einem Positionspapier der KDIGO sowie der UK Kidney Association ein zentraler Pfeiler der Akuttherapie einer schweren Hyperkaliämie bzw. einer Hyperkaliämie mit Vorliegen von EKG Veränderungen [1, 4, 156, 174].
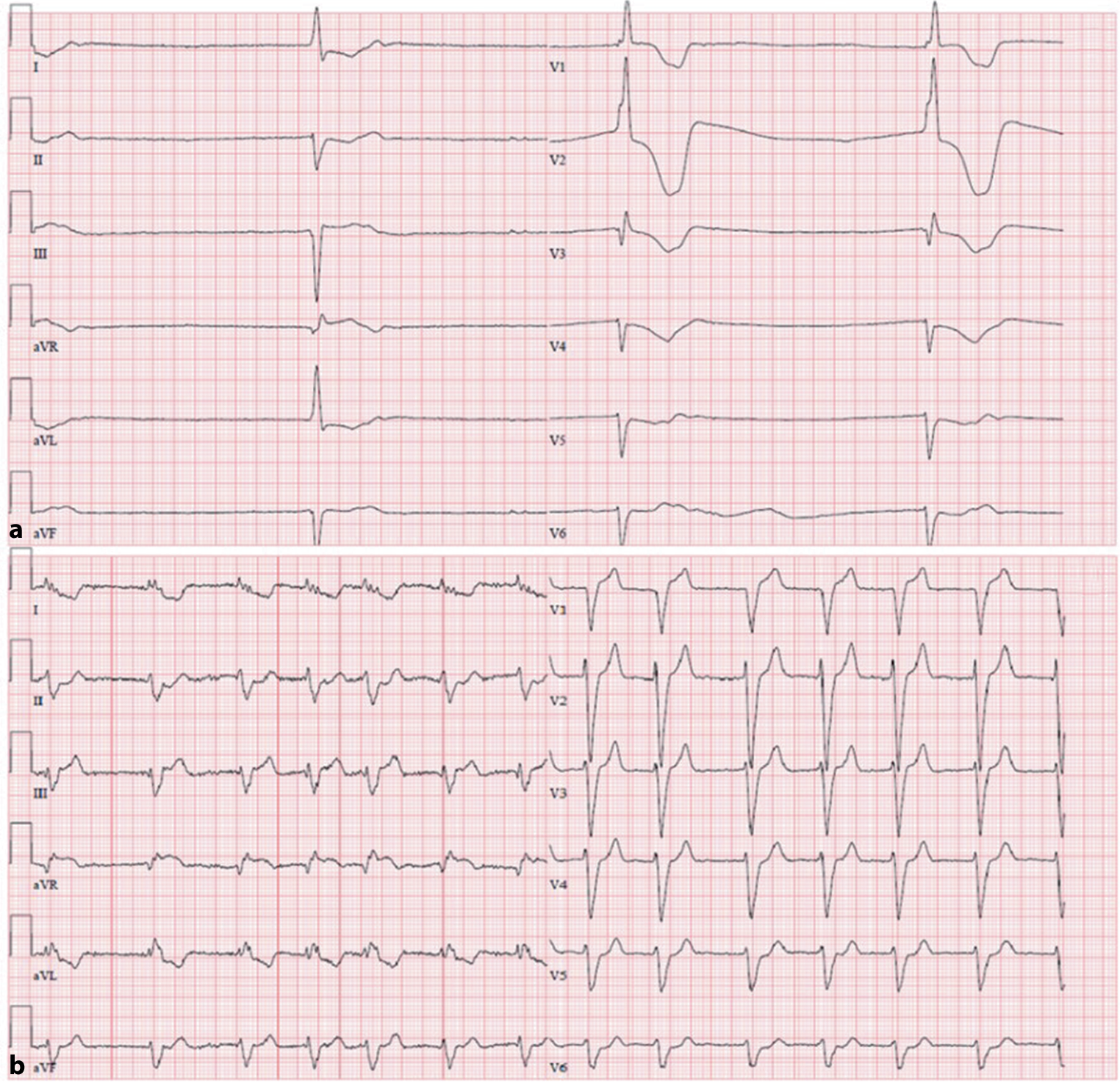
Die Infusion von Kalzium hat keinen Effekt auf die Kaliumkonzentration selbst, jedoch antagonisiert Kalzium die potenziell bedrohlichen Auswirkungen der Hyperkaliämie auf die Reizleitung. Als Grund dafür wurde in der älteren Literatur angegeben, dass sich das Ruhemembranpotenzial durch die Kalziumgabe wieder normalisierte (oder stabilisierte) [87]. Rezentere Studien deuten jedoch darauf hin, dass Kalzium durch die Bindung an spannungsabhängige Natriumkanäle deren Aktivität trotz erhöhten Ruhemembranpotenzials wiederherstellt. Dies ermöglicht wieder eine Depolarisation, da der hemmende Effekt der Hyperkaliämie antagonisiert wird [85, 175, 176]. Der Effekt von Kalziumsalzen bei Hyperkaliämie-assoziierten Störungen des Reizleitungssystems ist in Abb. 6 illustriert.
![Abb. 6 EKG bei schwerer Hyperkaliämie: vor/nach Therapie mit Kalziumsalzen. Effekt der Verabreichung von 30 ml Calciumgluconat auf das EKG einer Patientin mit schwerer, symptomatischer Hyperkaliämie ([S‑K+] 7,48 mmol/l). EKG: 25 mm/s, 10 mm/mV. a Vor der Gabe: Bradykardie, QRS-Verbreiterung, Absenkung der ST-Strecke, b nach der Gabe von Calciumgluconat: Normalisierung der Herzfrequenz (bei Vorhofflimmern), des QRS-Komplexes und der ST-Streckenveränderung](https://cdn.prod.website-files.com/62a1addc5dabff015c15ef63/69b9e19b3b7097dac87afa59_508_2026_2708_Fig6_HTML.jpeg)
Kalzium kann im Rahmen einer Hyperkaliämie in 2 Formulierungen verabreicht werden: Calciumchlorid oder Calciumgluconat. Calciumchlorid ist zwar phlebotoxischer, es wird ihm aber eine schnellere Wirkung zugeschrieben, da es nicht wie Calciumgluconat in der Leber metabolisiert werden muss, um freigesetzt zu werden [177].
Aufgrund des höheren Kalziumgehaltes ist die Initialdosis an 10 % Calciumchlorid mit 10 ml über einen Zeitraum von 2–5 min zu wählen, während sie für Calciumgluconat 30 ml beträgt [4, 174]. Der Verabreichungszeitraum für Calciumgluconat variiert in der Literatur zwischen 2 und 5 min in den American Heart Association (AHA) Guidelines sowie bis zu 15 min in den britischen ALS Guidelines [178] (RCUK Advanced Life Support Manual 8th Edition, May 2021). Auf Basis rezenter Evidenz erscheint es zentral zu sein, eine Dosis von 30 ml Calciumgluconat zu verabreichen, da es in einer Vielzahl an Fällen notwendig war, bei Gabe von 10 ml 10 % Calciumgluconat eine nochmalige oder sogar eine dritte Dosis an i.v.-Kalzium zu verabreichen, um einen Effekt zu erzielen [179]. Da die Wirkung nach 30–60 min abklingt, können auch repetitive Gaben von Kalzium notwendig sein, falls es in der Zwischenzeit durch andere Maßnahmen nicht möglich war, den Kaliumspiegel zu senken [156].
Kalziumsalze in klinischen Studien
Die Evidenz für die Gabe von Kalziumsalzen im Rahmen einer vital bedrohlichen Hyperkaliämie (inklusive Herz-Kreislauf-Stillstand) ist jedoch limitiert [180]: In 2 Tiermodellen mit Hyperkaliämie-induziertem Herz-Kreislauf-Stillstand zeigte sich durch die Gabe von Calciumchlorid keine erhöhte Rate an Return-of-spontaneous-Circulation (ROSC) bzw. Überleben [181, 182]. In einem klinischen Versuch bei Patient:innen mit Out-of-hospital-cardiac-Arrest mit pulsloser elektrischer Aktivität und EKG-Veränderungen, welche als suggestiv für eine Hyperkaliämie eingeschätzt wurden, zeigte sich unter Gabe von Kalzium keine erhöhte ROSC-Rate, und es wurde (bei jedoch sehr weitem Konfidenzintervall) sogar ein schlechteres Outcome diskutiert. Als klare Limitation ist hier jedoch zu nennen, dass das Vorliegen einer Hyperkaliämie nicht bestätigt war [183].
In einer Metaanalyse zu den verschiedenen Therapieoptionen einer Hyperkaliämie (mit/ohne Herz-Kreislauf-Stillstand) kamen die Autoren zu dem Schluss, dass es keine Evidenz für den Einsatz von Kalziumsalzen in der Therapie einer Hyperkaliämie geben würde [184].
Zumindest eine prospektive Studie aus der Türkei mit Patient:innen mit Hyperkaliämie ohne Kreislaufstillstand zeigte einen positiven Effekt von Calciumgluconat auf Hyperkaliämie-assoziierte Rhythmusstörungen im Sinne einer Rückbildung ebendieser [179].
Zusammengefasst ist die Evidenz für oder gegen den Einsatz von Kalziumsalzen bei Hyperkaliämie stark limitiert. Fest steht, dass eine Wirkung von Kalziumsalzen bei Hyperkaliämie sowohl anekdotisch als auch in Fallserien beschrieben wird bei gleichzeitig begrenzten unerwünschten Arzneimittelwirkungen. Auf der anderen Seite weisen die Studien mit negativen Daten relevante Limitationen auf, wie z. B. fehlende Daten zur konkomitanten Senkung des erhöhten Kaliums.
Kommentar
Der Einsatz von i.v.-Kalzium wird v. a. bei Patient:innen mit Kalium-assoziierten EKG-Veränderungen empfohlen (s. oben). Wahrscheinlich ist es sinnvoll, i.v.-Kalzium bei Patient:innen mit extremer Hyperkaliämie ([S-K+] > 7,0 mmol/l) auch ohne EKG-Veränderungen zu verabreichen, wenn Risikofaktoren für einen weiteren Kaliumanstieg oder Arrhythmien vorhanden sind. Dies dient dazu, die Zeit, bis Maßnahmen zur Kaliumsenkung wirken, zu überbrücken und damit die Wahrscheinlichkeit für Rhythmusstörungen zu reduzieren. Ähnliches gilt, wenn typische EKG-Veränderungen, die auf eine schwere Hyperkaliämie hinweisen (schwere Bradykardie, Sinuswellen-EKG), vorhanden sind, aber die Bestimmung der [S‑K+] noch nicht möglich war [156].
2. Kaliumshift
Zur Senkung der Kaliumkonzentration ist das Shifting von extra- nach intrazellulär eine Möglichkeit, welche rasch und komplikationsarm umgesetzt werden kann. Dafür stehen prinzipiell Insulin, Betamimetika sowie Natriumbikarbonat zur Verfügung. Üblicherweise werden diese Maßnahmen ab einem [S‑K+] > 6,5 mmol/l ergriffen.
Insulin
Wir empfehlen ab einem [S‑K+] > 6,5 mmol/l die Verabreichung von 5 Einheiten Insulin intravenös mit zeitgleicher Gabe von 25 g Glukose oder alternativ 10 Einheiten Insulin mit 50 g Glukose intravenös über 5–15 min. Bei Patient:innen mit relevanter Hyperglykämie (> 200 mg/dl) kann ein Verzicht der Glukosegabe erwogen werden. In jedem Fall empfehlen wir anschließend ein engmaschiges Glukosemonitoring (alle 30 min).
Insulin bewirkt einen Shift von Kalium nach intrazellulär über eine Steigerung der Aktivität der Na+-K+-ATPase [87]. Die intravenöse Gabe von Insulin beginnt nach etwa 15 min einen kaliumsenkenden Effekt zu entfalten, erreicht einen Peak nach 30–60 min und bewirkt eine Kaliumsenkung über ca. 4 h. Dem gegenüber steht eine etwas verzögerte, dafür länger anhaltende Wirkung von subkutan verabreichtem Insulin [87]. Die [S‑K+] kann so vorübergehend um etwa 1 mmol/l gesenkt werden. Die Kombination mit Betamimetika erhöht die Effektivität der Kaliumsenkung (Senkung um bis zu 1,5 mmol/l) [185].
Basierend auf der vorhandenen Evidenz, zeigt Insulin einen klaren und klinisch relevanten, wenngleich passageren Effekt auf die [S‑K+] in der Behandlung einer Hyperkaliämie: In einer rezenten Metaanalyse konnte anhand der Auswertung von über 50 Studien gezeigt werden, dass die Applikation von 5 Einheiten Insulin zu einer vergleichbaren Senkung des Kaliums führt wie die Verabreichung von 10 Einheiten Insulin (jeweils in Kombination mit Glukose) (−0,6 bis −1,2 mmol/l vs. −0,7 bis −1,4 mmol/l) [184]. Diese Daten bestätigen Ergebnisse eines systematischen Reviews aus dem Jahr 2016, welcher keinen Unterschied in der Veränderung der Kaliumkonzentration zwischen den verschiedenen Insulindosen fand, hingegen führte die höhere Insulindosis signifikant häufiger zu Hypoglykämien [186]. Zur Vermeidung von Hypoglykämien im Rahmen der Behandlung einer Hyperkaliämie wurde in einer US-amerikanischen Studie ein Protokoll eingeführt, welches anhand der Nierenfunktion und des Glukosewertes eine Anpassung der Insulindosis vorsah. In einer retrospektiven Auswertung dieser Studie zeigte diese Maßnahme jedoch keinen Effekt auf die Inzidenz einer Hypoglykämie [187]. Eine Ko-Verabreichung von 25–50 g Glukose intravenös wird bei Insulingabe zur Vermeidung von Hypoglykämien empfohlen [4, 186]. Bei Patient:innen mit einer relevanten Hyperglykämie (> 200 mg/dl) kann auf die Ko-Applikation nach Abwägung der Risiken verzichtet werden [4].
Grundsätzlich empfiehlt sich neben einer Kontrolle der [S‑K+] auch eine Glukosekontrolle etwa 30 min nach Insulingabe. In Folge muss der Blutzucker bis 5 h nach Ende der Insulin-Glukosetherapie alle 30 min evaluiert werden. Das Risiko für Hypoglykämien ist besonders erhöht bei älteren Patient:innen ohne Diabetes, mit AKI/CKD, Blutzucker < 120 mg/dl vor Therapiebeginn und niedrigem Körpergewicht. Andere Leitlinien empfehlen 10 IE Insulin und 25 g Glukose i.v., gefolgt von weiteren 25 g Glukose i.v. über 5 h um auch das späte Hypoglykämierisiko zu senken [156].
Eine wiederholte Therapie mit Insulin-Glukose bei Persistenz einer Hyperkaliämie (4 h nach der Initialtherapie) wurde nur in einer Studie untersucht und war in dieser mit einem erhöhten Mortalitätsrisiko assoziiert [188].
Anmerkung: 500 ml 5 % Glukose enthalten 25 g Glukose, 500 ml 10 % Glukose enthalten 50 g Glukose und 100 ml 33 % Glukose enthalten 33 g Glukose.
Betamimetika
Wir empfehlen bei [S‑K+] > 6,0–6,5 mmol/l und unter Abwägung etwaiger Kontraindikationen (Tachykardie, Arrhythmien, koronare Herzkrankheit) die Gabe von Salbutamol 10–20 mg inhalativ oder alternativ 0,5 mg intravenös als Kurzinfusion zur Senkung der [S‑K+]. Die Therapie kann mit einer Gabe von Insulin (und Glukose) kombiniert werden. Aufgrund des potenziellen Nebenwirkungsprofils empfehlen wir bei Risikopatient:innen ein zeitgleiches kardiales Monitoring.
Betamimetika führen zu einem Shift von Kalium nach intrazellulär über eine β2-Rezeptor-vermittelte Aktivierung der Na+-K+-ATPase [87]. Betamimetika werden in der Literatur häufig als Alternative oder zusätzliche Therapieoption zu Insulin und Glukose bei Hyperkaliämie angegeben [4, 189].
In einer rezenten Metaanalyse zu den verschiedenen pharmakologischen Therapieoptionen einer Hyperkaliämie konnte für eine Dosis von 10–20 mg inhalativ appliziertem Salbutamol ein kaliumsenkender Effekt von −0,9 mmol/l (95 % CI: −1,2, −0,7) innerhalb von 120 min gezeigt werden [184]. Hierbei wurden 7 Studien mit insgesamt 87 Patient:innen inkludiert. Für die Anwendung von 0,5 mg intravenösem Salbutamol als Kurzinfusion wurde ein kaliumsenkender Effekt von −1,0 mmol/l (95 % CI: −1,4, −0,6) beschrieben [184]. Unerwünschte Effekte beinhalten das Auftreten von Tachykardie und Tachyarrhythmien und potenziell myokardiale Ischämien bei Vorhandensein einer koronaren Herzkrankheit [87].
Aufgrund von Überlegungen hinsichtlich einer Inkonsistenz in der Wirkung von inhalativ applizierten Betamimetika wird diese Applikationsroute von manchen Autoren nur bei gleichzeitig angewandter Therapie mit einer alternativen kaliumsenkenden Therapie (z. B. Insulin/Glukose) empfohlen [87]. Diese Einschätzung wird durch Ergebnisse einer aktuellen Metaanalyse jedoch nicht gestützt [184].
Kommentar – Anmerkung für die Praxis
Salbutamol ist erhältlich: 1) z. B. als Sultanol Dosieraerosol® (GlaxoSmithKline GmbH & Co. KG, London, UK) (Cave: 1 Hub enthält nur ca. 0,1 mg Sultanol), 2) als Inhalationslösung (1 ml = 5 mg Sultanol); davon sollten 2 ml vernebelt werden, 3) als Ampullen (1 Ampulle mit 0,5 mg Sultanol), alternativ kann auch Terbutalin 0,5 mg verabreicht werden: entweder als Bolus, aber nur 0,25 mg Sultanol/Terbutalin in 10 ml NaCl langsam i.v. oder auch als s.c. Injektion mit 0,5 mg Sultanol/Terbutalin. Die kaliumsenkende Wirkung setzt nach ca. 30 min ein und hält zumindest 2 h an. Nichtselektive Betablocker reduzieren die kaliumsenkende Wirkung deutlich.
Bikarbonat
Aufgrund des vermutlich sehr limitierten kaliumsenkenden Effekts und des nicht unerheblichen Nebenwirkungsprofils empfehlen wir, die Gabe von Natriumbikarbonat ausschließlich bei Patient:innen mit schwerer Hyperkaliämie und konkomitanter schwerer hyperchloridämischer metabolischer Azidämie (pH < 7,2) als zusätzliche Therapie in Betracht zu ziehen.
Die intravenöse Gabe von Natriumbikarbonat im Rahmen einer schweren Hyperkaliämie ist theoretisch durch 3 Mechanismen gerechtfertigt [87, 181]: 1. Bei Vorliegen einer hyperchloridämischen metabolischen Azidämie kann es durch die alkalisierende Wirkung von Natriumbikarbonat zu einem Shift von Kalium nach intrazellulär kommen. 2. Das hyperosmolare Natriumbikarbonat führt zu einer intravaskulären Volumenexpansion mit konsekutiver Dilution der [S‑K+]. 3. Die hohe Natriumkonzentration verbessert die Phase der raschen Depolarisation durch eine Erhöhung des Natriumeinstroms (ähnlich wie Kalziumsalze) [190].
Die Evidenz für den Einsatz von Natriumbikarbonat in der Therapie einer schweren Hyperkaliämie ist als limitiert anzusehen. In der bereits genannten Metaanalyse konnte in den insgesamt 5 eingeschlossenen Studien kein kaliumsenkender Effekt gefunden werden [184]. Unerwünschte Wirkungen einer Gabe von Natriumbikarbonat sind Volumenüberladung, Hypernatriämie, eine Reduktion des ionisierten Kalziums sowie eine CO2-Retention [87].
3. Kaliumelimination
a. Diuretika
Der Einsatz von Diuretika, insbesondere i.v.-Schleifendiuretika, kann in der Therapie einer schweren Hyperkaliämie erwogen werden, sollte aber auf Patient:innen ohne zeitgleiche Hypovolämie beschränkt bleiben.
Die theoretische Basis für den Einsatz von Diuretika (Schleifendiuretika, Thiazid[-artige] Diuretika) in der Therapie einer schweren Hyperkaliämie liegt in der gesteigerten renalen Kaliumausscheidung. Die Effektivität kann limitiert sein, da bei Patient:innen mit schwere Hyperkaliämie häufig eine relevante Einschränkung der glomerulären Filtrationsrate vorhanden ist [45, 87]. Bislang gibt es keine Studie, welche die Wirksamkeit von Schleifen- oder Thiaziddiuretika in der Therapie einer schweren Hyperkaliämie untersucht hat [1]. Zumindest an gesunden Probanden (ohne Hyperkaliämie) konnte ein kaliuretischer Effekt mit verschiedenen Diuretika beobachtet werden [191].
In einzelnen Kliniken wird die Kombination von Furosemid (80 mg i.v.) + isotoner NaCl Lösung (500–1000 ml), im Sinne einer forcierten Kaliurese bei Patient:innen mit Euvolämie angewendet; obwohl aus pathophysiologischer Sicht diese Therapiestrategie nachvollziehbar ist, gibt es keine Evidenz bezüglich der Effektivität dafür.
Auf Basis der aktuellen Datenlage sehen wir für weitere potenzielle Therapien wie SGLT2-Hemmer oder Laxanzien in der initialen Therapie einer schweren Hyperkaliämie zu diesem Zeitpunkt keine Relevanz.
b. Kaliumbinder
Aufgrund der verzögerten Wirkung und des mutmaßlich interindividuell schwer abschätzbaren Effekts sind Patiromer und Natrium-Zirkonium-Cyclosilicat (SZC) ausschließlich als Zusatz zu den oben genannten Maßnahmen in der Behandlung einer schweren Hyperkaliämie anzusehen, insbesondere in der weiterführenden Therapie zur Vermeidung eines Kaliumrebounds.
Natrium-Polystyrol-Sulfonat (SPS) erhielt 1958 die FDA-Zulassung, seit etwa 10 Jahren existieren 2 neuere Präparate, Patiromer und SZC. Ein kaliumsenkender Effekt bei einer schweren Hyperkaliämie in unterschiedlicher Ausprägung konnte für die zur Verfügung stehenden Wirkstoffe in verschiedenen Studien nachgewiesen werden [192‐199]. Patiromer und SZC weisen gegenüber SPS ein günstigeres Nebenwirkungsprofil auf [87, 200]. Sowohl für SZC als auch für Patiromer gibt es nur kleine Studien, welche deren Effektivität zur raschen Kaliumsenkung nachweisen konnten [196, 201]. Einige Studien zur Therapie mit Kaliumbindern im akuten Setting sind noch nicht abgeschlossen [202, 203].
Es gilt zu beachten, dass sowohl SZC als auch SPS durch seinen Natriumgehalt bei Patient:innen mit HF ein erhöhtes Risiko für eine Ödembildung und kardiale Dekompensationen darstellt [204‐207]. Dies dürfte aber in der initialen Behandlungsphase wahrscheinlich weniger bedeutend sein als in der Langzeittherapie. SZC dürfte zudem auch in den ersten 6 h nach Therapiebeginn keinen Vorteil in der Kaliumsenkung gegenüber Patiromer haben [208, 209]. Bezüglich der Dosierung und Wirkung bzw. Nebenwirkungen s. Tab. 2 und Abschnitt CKD.

4. Therapie von Risikofaktoren
Wir empfehlen eine Suche nach provozierenden Faktoren (Medikamente, Diät, Komorbiditäten, Kaliumsupplemente) bei allen Patient:innen mit schwerer Hyperkaliämie; auch um das Risiko einer nochmaligen Hyperkaliämie zu reduzieren.
Provozierende Faktoren für die schwere Hyperkaliämie (s. Risikofaktoren und Red Flags) sollen identifiziert und nach Möglichkeit beseitigt werden [25, 153, 210‐216]. Dies beinhaltet eine detaillierte Durchsicht der aktuellen und rezenten Medikamente, Evaluierung der Komorbiditäten (CKD, DM, HF) und Erhebung der Ernährungsgewohnheiten. Ebenso kommt der Behandlung einer akuten Nierenfunktionseinschränkung eine hohe Priorität zu, da diese als klar kausaler Faktor anzusehen ist [45]. Eine temporäre Pausierung von RAAS-modifizierenden Medikamenten kann erwogen werden (v. a. bei Hypotonie). Es sollten andere Medikamente, welche ursächlich für die Hyperkaliämie verantwortlich sein könnten (NSAR, Trimethoprim …) pausiert werden; dies gilt auch für Kaliumsupplemente. In der Akutsituation sollten kaliumreiche Nahrungsmittel (z. B. Bananen, Smoothies) vermieden werden. Das Ziel ist es, zukünftige Episoden einer Hyperkaliämie zu vermeiden [1].
Kommentar
Im Fall einer potenziell lebensbedrohlichen Hyperkaliämie sollte – bei entsprechendem klinischem Kontext – auch das Vorhandensein einer Patientenverfügung geprüft werden, bevor weitreichende/invasive Maßnahmen (Intensivstation, Dialyse …) gesetzt werden.
5. Indikation zur Nierenersatztherapie
Bei allen Patient:innen mit terminaler Nierenerkrankung unter chronischer Nierenersatztherapie mit schwerer Hyperkaliämie sollte eine Hämodialyse zur Kaliumelimination durchgeführt werden [1,4,145]. Ebenso sollte bei Patient:innen mit therapierefraktärer (inklusive Rebound‑)Hyperkaliämie sowie im Kontext mit einer schweren akuten Nierenerkrankung (z. B. Anurie) eine Dialyse erfolgen. Die Indikation zur Nierenersatztherapie sollte mit einem/einer Facharzt/-ärztin für Nephrologie abgesprochen werden [1,4].
Da die Anlage eines Dialysekatheters und die Vorbereitung der Dialysemaschine Zeit benötigen (bis zu 1 h), müssen überbrückend andere Maßnahmen eingesetzt werden (Kalzium, Insulin-Glukose, Salbutamol) [156]. Es können intermittierende oder kontinuierliche Nierenersatztherapieverfahren (NET) angewendet werden:
Intermittierende Hämodialyse
Bei Patient:innen mit symptomatischer Hyperkaliämie und/oder [S‑K+] > 8,0 mmol/l wird eine Kaliumkonzentration im Dialysat von 1 mmol/l empfohlen (s. Abb. 7; [217]). Wird ein Dialysat [K+] von 1,0 mmol/l gewählt, muss der Patient mit einem EKG-Monitor überwacht werden und alle 30 min die [S‑K+] gemessen zu werden. Bei einer [S‑K+] < 7,0 mmol/l sollte auf ein Dialysat-Kalium von 2,0 mmol/l umgestellt werden. Unter der Dialyse kommt es rasch zum Abfall der [S‑K+] (ca. 1,0 mmol/l/h) [218]. Ein rascher Abfall der [S‑K+] während der HD kann Herzrhythmusstörungen auslösen, weshalb initial die [S‑K+] nicht unter 4,5 mmol/l gesenkt werden sollte. Es ist innerhalb von 6 h nach Ende der Dialysebehandlung in Abhängigkeit von der [S‑K+] bei Dialysestart mit einem Wiederanstieg der [S‑K+] um bis zu 70 % zu rechnen (je höher die [S‑K+] bei HD-Start, umso stärker der Rebound), was weitere Dialysebehandlungen (u. a. am selben Tag) nötig machen könnte [219, 220]. Zusätzliche Therapien mit Kaliumbinder können diesen Rebound vielleicht etwas abmildern. Mit dem Beginn der NET sollen alle Maßnahmen, die den Shift von Kalium in den IZR anregen, pausiert werden, um die Kaliumelimination mit der Dialyse zu erhöhen [218]. Eine Peritonealdialyse ist zwar eine alternative Möglichkeit zur Kaliumsenkung in dieser Situation, wird aber in westlichen Ländern fast ausschließlich nur bei prävalenten Peritonealdialysepatient:innen angewendet (limitierter Zugang zur akuten Anlage eines Peritonealdialysekatheters) [221]. Bei Peritonealdialyse kann die [S‑K+] durch rasche und hochvolumige Dialysatwechsel gesenkt werden [222].
![Abb. 7 Hämodialyse: Dialysat-[K+]-Konzentration bei Hyperkaliämie [217, 218]](https://cdn.prod.website-files.com/62a1addc5dabff015c15ef63/69b9e19b3b7097dac87afa49_508_2026_2708_Fig7_HTML.jpeg)
Kontinuierliche Nierenersatztherapieverfahren
Aufgrund der niedrigeren Blut- und Dialysatflüsse bei kontinuierlicher NET ist die Kaliumelimination etwas langsamer als bei einer intermittierenden HD. Es sollte entweder eine CVVHD oder CVVHDF angewendet werden. Die Absenkung der [S‑K+] kann bei kontinuierlicher NET deutlich verkürzt werden (45 vs. 120 min), wenn sehr hohe Dialysatflüsse (8 l/h) und ein kaliumfreies Dialysat verwendet werden [223]. Der Vorteil einer kontinuierlichen NET liegt in der Vermeidung eines Rebound-Effekts, da in der Regel über 48–72 h behandelt wird [220].
6. Monitoring bei schwerer Hyperkaliämie
Wir empfehlen, Patient:innen mit schwerer Hyperkaliämie zu monitorisieren (EKG, Herzfrequenz, Blutdruck, SpO2), bis die Hyperkaliämie normalisiert oder deutlich rückläufig ist, insbesondere bei initialem Vorhandensein von EKG-Veränderungen. Eine engmaschige Kontrolle der Kaliumkonzentration ist bei jeder moderaten und schweren Hyperkaliämie erforderlich. Bei Gabe von Insulin sollte eine Kontrolle der Blutglukose zur Vermeidung einer Hypoglykämie erfolgen.
EKG-Monitoring
Patient:innen in der Notaufnahme mit moderater oder schwerer Hyperkaliämie sollen monitorisiert bleiben, bis der Kaliumwert normalisiert oder der Schweregrad reduziert wurde (Zielwerte [S‑K+] < 5,0 mmol/l) [4]. Dies ist insbesondere bei schwerer Hyperkaliämie, Vorhandensein von EKG-Veränderungen, bei kardiorespiratorischer Beeinträchtigung oder bei Risikopatient:innen mit moderater Hyperkaliämie erforderlich (s. unten). Retrospektive Daten implizieren, dass eine Verlegung außerhalb eines Überwachungsbereiches bei einer Kaliumkonzentration ≥ 5,5 mmol/l mit einem schlechteren Outcome assoziiert sein könnte [173].
Anmerkung
In der Praxis können wahrscheinlich nicht alle Patient:innen mit einer [S‑K+] > 6,0 mmol/l adäquat überwacht werden. Risikopatient:innen für einen komplizierten Verlauf sollten jedoch identifiziert und strikt überwacht werden, selbst wenn nur eine moderate Hyperkaliämie vorhanden ist:
- Patient:innen mit Risiko für raschen weiteren Anstieg der [S‑K+]: Rhabdomyolyse, Tumorlyse, akutes Nierenversagen oder Schock,
- Patient:innen mit hohem Risiko für Herzrhythmusstörungen: strukturelle Herzerkrankung, sowie zusätzliche Hypokalziämie oder Hypomagnesiämie [224].
Asymptomatische Patient:innen, ausschließlich mit moderater und vorbekannter Hyperkaliämie ohne zusätzliche Risikofaktoren oder akute Erkrankung, können bei fehlenden Ressourcen auch ohne Monitoring behandelt werden.
Kontrolle der [S-K+]
Bei schwerer Hyperkaliämie sollte 1 und 2 h nach Einleitung der medikamentösen Maßnahmen die [S‑K+] kontrolliert werden, um die Effektivität der Maßnahmen zu überprüfen [156]. Weitere Kontrollen nach 4 und 6 h dienen zur Kontrolle eines möglichen Rebounds nach medikamentösem Kaliumshifting in den IZR [4, 225, 226]. Die Kontrollen sind durchzuführen, bis die [S‑K+] normalisiert ist bzw. ein klarer Trend hin zur Normokaliämie absehbar ist [4]. 24 h nach Normalisierung der [S‑K+] sollte eine abschließende Messung erfolgen. Hier ist anzumerken, dass trotz Beendigung der Therapie mit Spironolacton aufgrund der langen Wirkdauer (im Vergleich zur Eplerenon und v. a. Finerenon) auch später noch Hyperkaliämien beobachtet werden können. Die Kontrolle der Blutglukose ist bei Gabe von Insulin/Glukose ebenfalls erforderlich.
Therapie bei milder bis moderater Hyperkaliämie
Eine einheitliche Definition für die chronische Hyperkaliämie existiert nicht [99]. Während akute Hyperkaliämien meist durch klinisch offensichtliche Ereignisse bedingt sind, ist eine chronische Hyperkaliämie durch eine milde-moderate Erhöhung der [S‑K+] > 5,0 mmol/l, fehlende Symptome sowie das Fehlen einer akuten Erkrankung charakterisiert und ist deshalb oft ein Zufallsbefund im Rahmen von Routineuntersuchungen [1]. Es wird deshalb der Begriff der milden bis moderaten Hyperkaliämie gegenüber dem Begriff der chronischen Hyperkaliämie bevorzugt.
Aufgrund der steigenden Mortalität bei [S‑K+] > 5,5 mmol/l sollte oberhalb dieses Wertes ein Therapiekonzept für die Hyperkaliämie angestrebt werden [54, 57, 227]. Anzumerken ist, dass die meisten Interventionsstudien bloß die Effizienz einer Kaliumsenkung und nur einzelne Studien den Effekt der Kaliumsenkung auf die Mortalität untersuchten [228]. Bei schweren Hyperkaliämien ([S‑K+] > 6,0–6,5 mmol/l) sind meistens eine stationäre Aufnahme und akute Intervention (s. schwere Hyperkaliämie) notwendig [156]. Im Rahmen des Aufenthaltes sollte, falls es sich tatsächlich um eine chronische Hyperkaliämie gehandelt hat, ein Konzept für die langfristige Therapie erstellt werden.
Bei der Behandlung der chronischen Hyperkaliämie sind grundsätzlich folgende Therapieoptionen möglich:
- Ernährungsempfehlungen zur Kaliumzufuhr,
- Erhöhung der intestinalen Kaliumelimination,
- Erhöhung der renalen K+-Elimination durch Erhöhung der Na+-Anflutung an den distalen Tubulus,
- Erhöhung der Aldosteronwirkung.
Ziel ist es, die [S‑K+] auf < 5,0–5,5 mmol/l zu senken, um damit das Risiko für Arrhythmien zu reduzieren, welche hauptsächlich für die akute Mortalität verantwortlich gemacht werden. Die Erhöhung der Langzeitmortalität ist aber nicht nur auf das Risiko für Herzrhythmusstörungen, sondern auch auf die Gründe für die Hyperkaliämie zurückzuführen, v. a. auf die Komorbiditäten. Eventuell kann die Kaliumsenkung z. B. durch Kaliumbinder auch langfristig positive Auswirkungen auf die kardiovaskuläre Situation haben, da diese zu einem Abfall des Aldosterons führt [229]. Einzig negative Auswirkung einer geringeren Aldosteronkonzentration ist ein verringerter Shift von K+ in den IZR.
Es werden in Folge die Therapiemöglichkeiten bei chronischer Hyperkaliämie in Anlehnung an die Komorbiditäten bzw. Ursachen dargestellt.
Chronische Therapie der Hyperkaliämie bei chronischer Nierenerkrankung ohne Nierenersatztherapie
Ernährungsempfehlungen
Die Reduktion der Kaliumzufuhr in Situationen, bei denen die renale Kaliumeliminationskapazität eingeschränkt ist, erscheint logisch, ist aber nicht bei allen Patient:innen unbedingt erforderlich bzw. effektiv.
Es wird die Erhebung der aktuellen Kaliumzufuhr im Rahmen einer professionellen Ernährungsberatung („food record“) empfohlen. Eine Reduktion der Kaliumzufuhr bei einer hohen Kaliumzufuhr > 100 mmol/Tag ist angezeigt. Bevorzugte Kaliumquellen sollten Gemüse und Obst mit hohem Faseranteil sein. Vermieden werden sollen Kalium aus prozessierten Lebensmitteln, aus tierischer Herkunft und Kaliumsupplemente, sowie Diätsalz (KCl). Durch Kochen kann der Kaliumgehalt verschiedener Lebensmittel deutlich reduziert werden.
Die Kaliumzufuhr bei Patient:innen mit CKD ist traditionell niedrig. Es nehmen weniger als 15 % der Patient:innen die für Nierengesunde empfohlene Menge an Kalium (> 100 mmol/d) zu sich [230]. Observationsstudien bei Patient:innen ohne/mit CKD oder mit Dialyse zeigen eine schwache Korrelation zwischen der täglichen Kaliumzufuhr und der [S‑K+] [70, 230‐234]. Eine niedrige Zufuhr an Kalium bei CKD ist mit einer höheren Mortalität assoziiert, da offensichtlich dadurch v. a. in Früchten und Gemüse enthaltene Nährstoffe in geringerem Ausmaß zugeführt werden [1].
Dennoch kann ein Effekt der Kaliumzufuhr auf die [S‑K+] beobachtet werden. In einer kleinen, randomisierten Studie (n = 29), welche den Effekt einer kaliumarmen (40 mmol/d) vs. kaliumreichen Diät (100 mmol/Tag – Zusammensetzung wie bei DASH-Diät) bei Patient:innen mit gering eingeschränkter Nierenfunktion untersuchte (CKD G3), war das Risiko für eine Hyperkaliämie 2,5-mal höher (K+-arm vs. K+-reich: 7 vs. 17 % entwickelten eine Hyperkaliämie) als in der Gruppe mit niedriger Kaliumzufuhr [235]. Ähnliche Ergebnisse konnten in der Run-in-Phase einer Studie beobachtet werden, bei der Patient:innen mit CKD G4, zusätzlich tgl. 40 mmol KCl erhielten und es zu einem Anstieg der [S‑K+] um 0,4 mmol/l kam bzw. 11 % der Patient:innen eine Hyperkaliämie entwickelten [236].
Umgekehrt hat die Einleitung einer Ernährungstherapie nach dem ersten Auftreten einer Hyperkaliämie ([S‑K+] > 5,0 mmol/l) bei CKD G3–4 nur einen geringen Effekt auf zukünftige Episoden von Hyperkaliämien. Immerhin entwickelten 56 % innerhalb von 6 Monaten eine neuerliche Episode einer Hyperkaliämie [237]. Ein Grund dafür kann die fehlende Adhärenz sein, die sich aus den komplexen Anleitungen zur Durchführung der Diätmaßnahmen erklärt: Was darf ich in welcher Menge essen? Was muss ich kochen? Wo verstecken sich Kaliumsalze? etc.
Diese Daten zeigen, dass eine Adaptierung der Art der Kaliumzufuhr und das Vermeiden von höheren Kaliummengen (> 100 mmol/d) bei einzelnen Patient:innen mit CKD und chronischer Hyperkaliämie notwendig sein kann, obwohl die Evidenz dafür nicht gut ist. Auch reduziert ein geringerer Konsum von Lebensmitteln mit sehr hohem Kaliumgehalt den postprandialen Anstieg der [S‑K+] [115]. Dazu ist aber eine professionelle Beratung notwendig, die auch die aktuelle Kaliumzufuhr klinisch erheben soll (Ernährungsprotokoll).
Die Adaptierung der Art der Kaliumzufuhr bedeutet konkret: Kalium aus Früchten und Gemüse mit einem hohen Faseranteil sollten bevorzugt werden, da sie zu einem geringeren Ausmaß resorbiert werden (50–60 %), alkalihaltig sind und viele Kohlehydrate beinhalten, was den postprandialen Anstieg der [S‑K+] vermindert („shift“) und die renale Elimination erleichtert. Zudem beschleunigt der Faseranteil die Kolontransitzeit und damit die intestinale Kaliumelimination. Dies konnte in einer kleinen Studie an Patient:innen mit CKD G4 bestätigt werden [238]. Dem gegenüber sollte Kalium aus tierischen Quellen, verarbeiteten Lebensmittel (welche als Konservierungsmittel Kaliumsorbit [E202], Kaliumphosphat [E450], Kaliumsulfat [E224] etc. enthalten) und Kaliumchlorid (Diätsalz), die eine höhere Bioverfügbarkeit haben (tierische Quellen: 70–90 % bzw. alle anderen: 90 %) und azidifizierend wirken, vermieden werden [99, 239, 240].
Weiters kann das Kochen von Lebensmitteln den Kaliumgehalt von verschiedenen kaliumreichen Lebensmitteln (z. B. Kartoffel) reduzieren [67]. Derzeit laufende Studien wie der „DK-Lib-CKD-trial“, in dem direkt zwischen einer Kaliumzufuhr von 2 g vs. 3,5 g verglichen wird, können vielleicht in Zukunft neue Informationen liefern [241].
Adaptierung der Medikation
Medikamente ohne prognostischen Benefit, welche den Kaliumspiegel anheben (z. B. NSAR, Trimethoprim, Kaliumsupplemente), sollten abgesetzt werden. Ein Absetzen der RAASi-Therapie aufgrund einer Hyperkaliämie ist ausschließlich bei einer persistierenden [S‑K+] > 6,0 mmol/l trotz Ausschöpfung kaliumsenkender Therapieoptionen indiziert.
Das Absetzen von RAASi bei Hyperkaliämie und einer eGFR < 30 ml/min/1,73 m2 ist mit einer erhöhten Mortalität assoziiert und sollte deshalb möglichst vermieden werden, indem andere Maßnahmen, z. B. Kaliumbinder, eingesetzt werden [242, 243]. Nur bei persistierender Hyperkaliämie (> 6,0 mmol/l) trotz dieser Maßnahmen sollten die RAASi-Therapie in der Dosis reduziert oder abgesetzt werden.
Kaliumelimination
Kaliumbinder (Patiromer oder SZC) sollen bei Patient:innen mit CKD + [S‑K+] > 6,0 mmol/l eingesetzt werden, v. a. um den Einsatz bzw. die maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen.
Schleifen- und Thiaziddiuretika können zur Senkung der [S‑K+] eingesetzt werden, wenn primär bereits eine Indikation dafür besteht (Hypervolämie, Hypertonie, Proteinurie), ebenso SGLT‑2-Hemmer.
Laxanzien zur Stuhlregulation bei Obstipation können die [S‑K+] ebenfalls senken.
Der Einsatz von Puffersubstanzen (wie Natriumhydrogenkarbonat) zur Senkung der [S‑K+] kann aufgrund der geringen Wirkung und des Risikos der Natriumbelastung nicht empfohlen werden.
Kaliumbinder
Kaliumbinder wirken unabhängig von der oralen Kaliumzufuhr und werden mittags oft deshalb eingenommen, um potenzielle Interaktionen (Resorptionshemmung) mit anderen Medikamenten zu vermeiden. Sie binden Kalium, indem ein anderes Kation (Na+, Ca2+, H+) freigesetzt wird (Kationentauscher); die Wirkung setzt nach 1–7 h ein. Damit kann die intestinale Kaliumelimination um bis zu 1 g (25 mmol) tgl. erhöht werden [244] (Eigenschaften der Kaliumbinder s. Tab. 2). Allerdings gibt es keine Daten, die zeigen, dass Kaliumbinder den postprandialen Anstieg der [S‑K+] reduzieren, was aufgrund ihrer Wirkungsweise auch unwahrscheinlich ist [115].
Bei CKD (G3–5, mit/ohne DM und RAASi) ist die Effizienz der Therapie (für bis zu einem Jahr) v. a. mit dem intestinalen Kaliumbinder Patiromer nachgewiesen worden [245‐247]. Auch SZC (bei RAASi) ist wirksam, sodass über 75 % der Patient:innen (teilweise mit DM und HF) mit ca. 10 g SZC/Tag oft innerhalb von 48 h eine [S‑K+] < 5,0 mmol/l erreichen, und das ohne der Vorgabe einer speziellen kaliumarmen Diät [248‐250]. Die maximale in Studien beobachtete effektive Behandlungszeit für SZC betrug 12 Monate [251]. Die NEUTRALIZE-Studie zeigte zusätzlich eine Besserung des S‑Bikarbonats unter SZC [252]. Zumindest in einer Kohortenstudie konnte ebenfalls ein positiver Effekt einer Langzeittherapie mit Patiromer auf die Mortalität beobachtet werden [228]. Die STABILIZE-CKD-Studie mit dem Ziel, den Effekt von SZC bei CKD und RAASi-Therapie auf die Mortalität zu untersuchen, wurde wegen Rekrutierungsproblemen abgebrochen (ClinicalTrials.gov ID NCT05056727).
Insgesamt sind die Daten gerade ausreichend, um den Einsatz von Patiromer/SZC bei Patient:innen mit CKD + [S‑K+] > 6,0 mmol/l zu empfehlen, v. a. um den Einsatz bzw. die maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen. Die zu erwartende Senkung der [S‑K+] liegt bei etwa 0,4–1,0 mmol/l. Als spezielles Risiko von SZC muss die Natriumbelastung bei Patient:innen mit zusätzlicher Herzinsuffizienz erwähnt werden, welche in Abhängigkeit von der Dosis das Risiko für Ödembildung und kardiale Dekompensationen erhöht [204, 205, 207, 253].
Nicht sicher ist, ob die Therapie mit intestinalen Kaliumbindern eine liberalere Kaliumzufuhr ermöglicht, da die meisten Studien zusätzlich eine kaliumreduzierte Kost im Therapieprotokoll hatten [115, 156]. Zumindest in einer Studie konnte gezeigt werden, dass mit einer Kaliumbindertherapie auch eine kaliumreichere Kost zugeführt werden kann, ohne das Risiko für eine Hyperkaliämie zu erhöhen [254]. SZC kann sich zusätzlich durch seine intestinale Bindung von NH4 positiv auf eine metabole Azidose auswirken [252].
Die Verwendung der neueren intestinalen Kaliumbinder wie Patiromer oder SZC sollte gegenüber von Natrium-Polystyrol-Sulfonat bevorzugt werden [200]. Dies beruht nicht auf der fehlenden Wirkung, sondern auf: a) dem erhöhten Risiko für potenziell schwere Nebenwirkungen (V. a. Darmwandnekrosen bei glz. Sorbitol), b) der etwas höheren Rate an milden gastrointestinalen Nebenwirkungen bzw. des unangenehmen Geschmacks und c) v. a. der damit verbundenen niedrigen Therapieadhärenz [156, 255‐259]. Wahrscheinlich ist der negative Effekt von Natrium-Polystyrol-Sulfonat zeitabhängig, da keine Unterschiede an gastrointestinalen Nebenwirkungen im Vergleich zu Patiromer oder SZC bei hospitalisierten Patient:innen beobachtet werden konnte [260].
Diuretika
Bei guter Restnierenfunktion können Thiaziddiuretika (v. a. Chlortalidon) und Schleifendiuretika die renale Kaliumelimination erhöhen [87, 261, 262]. Insgesamt dürfte der kaliuretische Effekt von Schleifendiuretika besser sein als der von Thiaziddiuretika; es ist eine Absenkung des [S‑K+] um 0,6 vs. 0,3 mmol/l zu erwarten [38]. Obwohl es für diese Indikation keine Interventionsstudien gibt, konnte z. B. in Studien beobachtet werden, dass der Einsatz von Thiaziddiuretika oder Schleifendiuretika das Risiko für eine Hyperkaliämie (in der FIDELIO-DKD um ca. 24 %) senkt [29, 168].
Durch eine sequenzielle Nephronenblockade (Kombination Schleifendiuretikum und Thiaziddiuretikum) kann der kaliumsenkende Effekt noch stärker ausgeprägt sein [263]. Diese wurde aber nicht gezielt in Studien zur Therapie der Hyperkaliämie untersucht. Der Einsatz ist nur bei Patient:innen mit Hypertonie und Hypervolämie möglich, Hypovolämien sollten unbedingt verhindert werden [139, 264].
Auch für SGLT2‑Hemmer ist ein kaliumsenkender Effekt beschrieben, der jedoch geringer als unter Diuretika sein dürfte. In verschiedenen Risikogruppen (CKD, DM, RAASi-Therapie) konnte im Gesamten die Rate an schweren Hyperkaliämien um 16 % reduziert werden, ohne das Risiko für Hypokaliämien zu erhöhen [265‐267]. In der FIDELIO-DKD-Studie war die Rate der Hyperkaliämien unter SGLT-2-Hemmer + ns-MRA deutlich geringer als ohne (8,1 vs. 18,7 %) [29]. Obwohl es für den gezielten Einsatz von SGLT-2-Hemmern zur Therapie der Hyperkaliämie keine Evidenz gibt, empfiehlt sich die Therapie eines SGLT-2-Hemmers zumindest, wenn ein ns-MRA verwendet wird, da die Kombination auch kardio- und nephroprotektiv ist [167, 268].
Laxanzien
Obstipation ist bei Patient:innen mit CKD mit höherem Kaliumspiegel assoziiert. Der Einsatz von Laxanzien ist hingegen mit niedrigeren Kaliumwerten assoziiert, was den Einsatz von Laxanzien bei CKD-assoziierter Hyperkaliämie und Obstipation sinnvoll macht [269].
Puffertherapie
Die metabole Azidose bei CKD ist mit Hyperkaliämie assoziiert. Studien an Patient:innen (CKD ohne Dialyse) mit Puffersubstanzen konnten zeigen, dass bei Patient:innen mit metaboler Azidose unter Puffertherapie die [S‑K+] niedriger (um ca. 0,7 mmol/l) war als in der Placebogruppe [270]. Diese Beobachtung konnte von anderen Studien jedoch nicht bestätigt werden [271]. Da der Einsatz von Na+-Bikarbonat als Puffersubstanz zudem keinen zusätzlich positiven Effekt auf CKD-Progression oder Mortalität [272], jedoch potenzielle Nebenwirkungen durch die Natriumbelastung zeigt, ist ein Einsatz zur Behandlung der Hyperkaliämie bei einem Serum-Bikarbonat > 18 mmol/l primär nicht zu empfehlen.
Kommentar – Hinweis für die Praxis
Bei CKD und milder Hyperkaliämie empfehlen wir folgende Vorgehensweise: zuerst Korrektur der leicht modifizierbaren Faktoren: Absetzten von Medikamenten, welche die [S‑K+] erhöhen können (mit Ausnahme der RAASi, evtl. Dosisreduktion überlegen), Einsatz von Schleifen‑/Thiaziddiuretika bei Hypervolämie/Hypertonie, Puffertherapie nur bei schwerer Azidose, Behandlung einer Obstipation, Start einer SGLT2-Hemmer-Therapie sowie Diätberatung, um einen postprandialen Kaliumanstieg durch zu hohe Kaliumbelastung zu vermeiden. Falls dies zu keinem Absinken der [S‑K+] < 5,5 mmol/l führt oder primär eine moderate Hyperkaliämie besteht, sollten intestinale Kaliumbinder zum Einsatz kommen [99].
Chronische Therapie der Hyperkaliämie bei Nierenersatztherapie
Eine extrakorporale Nierenersatztherapie (Hämodialyse [HD] und Peritonealdialyse [PD]) kann v. a. durch Diffusion relevante Mengen an Kalium eliminieren. Dabei ist die Menge der Kaliumelimination pro Zeiteinheit abhängig vom Kalium-Konzentrationsgradienten zwischen Blut und Dialysat. Mit der HD können pro Behandlung (ca. 4 h) 70–100 mmol Kalium eliminiert werden [145]. Da die HD nur 3‑mal/Woche durchgeführt wird, ist bei anurischen Patient:innen eine zusätzliche Kaliumelimination über den Darm erforderlich, um die Kaliumhomöostase aufrechtzuerhalten [273]. Bei Patient:innen mit chronischer Hämodialyse sind prädialytische [S‑K+] > 6,5 mmol/l nicht ungewöhnlich. Die Kaliummessung erfolgt dabei meistens bei Start der Dialysebehandlung. Sind die Patient:innen asymptomatisch, ist nur bei [S‑K+] > 7,5–8,0 mmol/l ein EKG-Monitoring empfohlen, da eine Kaliumsenkung mit der Dialyse sehr rasch erfolgt. Nach Ursachen der Hyperkaliämie (wie Diätfehler, unzureichende Dialysequalität …) ist gezielt zu suchen.
Mittels PD wird ebenfalls über Diffusion pro Woche eine ähnliche Menge an Kalium eliminiert wie mit HD (ca. 30–40 mmol/Tag, pro Woche somit über 200 mmol); die üblicherweise bessere Restnierenfunktion stellt hier einen bedeutenden zusätzlichen Faktor der Kaliumelimination dar [274]. PD-Patient:innen entwickeln deshalb erst mit dem Rückgang der Restnierenfunktion eine Hyperkaliämie, sodass diese in den ersten 12 Monaten nach Start der PD deutlich seltener (ca. 10–15 %) auftritt. Bei längerer Therapiedauer kann bei bis zu 50 % der Patient:innen eine Hyperkaliämie vorliegen [275, 276].
Nierenersatztherapie
Bei der chronischen Hämodialyse sollte bis zu einer prädialytischen [S‑K+] von 8,0 mmol/l die Dialysat-Kaliumkonzentration nicht < 2,0 mmol/l abgesenkt werden. Bei der Peritonealdialyse kann eine Intensivierung der Behandlung (mehr Behandlungsvolumen) die Kaliumelimination erhöhen.
An der HD kann durch Änderung der Dialysat-Kaliumkonzentration (Standard 2,0–4,0 mmol/l) die Kaliumelimination durch Diffusion gesteuert werden. Ältere Daten weisen auf ein erhöhtes Arrhythmierisiko bei der Verwendung von niedrigen Dialysat-[K+] hin, was aber darauf zurückzuführen ist, dass auch Patient:innen mit normalen [S‑K+] in diese Studien inkludiert wurden [277, 278]. Andererseits kann nur eine niedrige Dialysat-[K+] adäquate Kaliummengen eliminieren [279]. Rezentere Daten bei chronischen HD-Patient:innen mit Hyperkaliämie zeigen keinen Hinweis auf eine erhöhte Mortalität bei Verwendung von niedrigen Dialysat-[K+] (bis 1 mmol/l). Es sollte deshalb die Berechnung der Dialysat-[K+] anhand der Abb. 7 durchgeführt werden. In der Praxis können jedoch bei einzelnen Patient:innen trotz prädialytischer [S‑K+] > 6,0 mmol/l bei Verwendung von Dialysat-[K+] 2,0 mmol/l Vorhofflimmerarrhythmien beobachtet werden. Bei diesen könnte die Kombination aus Dialysat-[K+] 3,0 mmol/l und einer interdialytischen Therapie mit intestinalem Kaliumbinder (SZC) überlegt werden, da diese Kombination sich positiv auf das Arrhythmierisiko auswirkt [280]. Wichtig ist, dass es nach einer intermittierenden Hämodialysebehandlung zu einem Rebound-Phänomen kommt; je höher das prädialytische [S‑K+], desto höher steigt die [S‑K+] 3–4 h nach Ende der Dialyse wieder an. Beispiel: Vor der HD: [S‑K+] 7,0 mmol/l, unmittelbar nach HD-Ende [S‑K+] 4,0 mmol/l, 4 h nach der HD [S‑K+] 6,0 mmol/l [219].
Bei der Peritonealdialyse (Dialysat-Kalium immer 0 mmol/l) kann durch Intensivierung der Therapie (höheres Behandlungsvolumen) die Kaliumelimination ebenfalls erhöht werden, oder intestinale Kaliumbinder können angewendet werden, obwohl es dafür noch keine ausreichenden Studiendaten gibt.
Ernährungsempfehlungen
Erhebung der aktuellen Kaliumzufuhr im Rahmen einer professionellen Ernährungsberatung („food record“). Reduktion der Kaliumzufuhr bei einer hohen Kaliumzufuhr > 100 mmol/Tag. Es gelten dieselben Diätempfehlungen bezüglich der Art und Menge der Kaliumzufuhr wie bei CKD ohne Dialyse.
In einigen (älteren) Leitlinien wird bei Dialysepatient:innen eine maximale Kaliumzufuhr von 3 g (ca. 75 mmol/Tag) empfohlen. Dies ist in den aktuellen Stellungnahmen modifiziert worden, mit einem Schwerpunkt auf die Art der Kaliumzufuhr und keiner generellen Kaliumrestriktion, was auch für Dialysepatient:innen gültig ist [1].
Auch bei Dialysepatient:innen gibt es keine bzw. nur eine schwache Korrelation zwischen Kaliumzufuhr und prädialytischen [S‑K+] [231, 281, 282]. Vor allem in der DIET-HD-Studie, bei der eine große Anzahl an Hämodialysepatient:innen mit einer Kaliumzufuhr von < 64 bis > 128 mmol/Tag konnte keine Korrelation mit der [S‑K+] bzw. dem Auftreten von Hyperkaliämien beobachtet werden. Es konnte aber auch kein protektiver Effekt einer hohen Kaliumzufuhr gezeigt werden, obwohl bei den Patient:innen mit hoher Kaliumzufuhr v. a. pflanzliche Kaliumquellen dominierten [231]. In einer früheren Studie konnte sogar ein leicht negativer Effekt einer hohen Kaliumzufuhr beobachtet werden, wobei hier v. a. Kalium aus tierischen Quellen oder über Konservierungsstoffe konsumiert wurden [282]. Nur eine kleine, aber randomisiert kontrollierte Studie zeigte eine gering höhere [S‑K+] (4,8 vs. 4,6 mmol/l), wenn eine normale Diät mit einer Kaliumrestriktion verglichen wurde [283].
Kaliumbinder
Kaliumbinder (Patiromer oder SZC) können bei Patient:innen mit NET + [S‑K+] > 6,0 mmol/l eingesetzt werden.
Bei HD-Patient:innen mit Hyperkaliämie führt die Therapie mit SZC (Start 5 g bis max. 15 g/Tag) am Nicht-Dialysetag im Vergleich zu Placebo bei fast 42 % der Patient:innen (vs. 1 % bei Placebo) zu einer Senkung der prädialytischen Kaliumwerte (< 5,5 mmol/l) [284]. Die Effektivität konnte über einen längeren Zeitraum und in anderen Studien bestätigt werden [251, 285]. Ein mögliches Problem der Therapie mit SZC ist die Natriumbelastung, wobei in der Studie kein Einfluss auf die interdialytische Gewichtszunahme beobachtet wurde [284]. Die Therapie reduziert aber trotz effektiver Kaliumsenkung nicht Arrhythmie-assoziierte kardiovaskuläre Endpunkte [286]. Patiromer senkt ebenfalls bei hyperkaliämischen Dialysepatient:innen die [S‑K+] [258, 287, 288]. Daten zur Anwendung von Patiromer oder SZC an der Peritonealdialyse sind nicht ausreichend vorhanden, um eine Beurteilung hinsichtlich der Effektivität abzugeben, es ist aber davon auszugehen, dass sie ähnlich gut wie bei Hämodialysepatient:innen wirken [285].
Weitere Therapiemaßnahmen
Vermeidung von Obstipation: In kleinen Studien konnte die Verabreichung von Laxanzien (z. B. Bisacodyl) die Wahrscheinlichkeit einer Hyperkaliämie deutlich reduzieren [289, 290].
Schleifendiuretika: Für eine kaliumsenkende Wirkung von Schleifendiuretika an der Hämodialyse gibt es widersprüchliche Daten, wobei die DOPPS-Analysen seltener schwere Hyperkaliämien unter Diuretikatherapie zeigten [291, 292]. Auch können hyperkaliämische Dialysepatient:innen zusätzlich einen (hyporeninämischen) Hypoaldosteronismus aufweisen [293]. Prinzipiell ist aber Fludrocortison in der Behandlung einer Hyperkaliämie an der Hämodialyse nicht sehr wirkungsvoll [294].
Zur Vorbeugung von Nüchternhyperkaliämien empfiehlt es sich, vor operativen Eingriffen die Patient:innen mit einer glukosehaltigen Infusion zu behandeln [295].
Therapie der Hyperkaliämie unter RAAS-Blockade
Kaliumbinder (Patiromer oder SZC) können bei Patient:innen unter RAASi + [S‑K+] > 5,5 mmol/l eingesetzt werden, v. a. um den Einsatz bzw. die maximale Dosierung einer kardio- und nephroprotektiven RAASi-Therapie zu ermöglichen. Liegt die [S‑K+] unter Ausschöpfung der K+-senkenden Therapie aber > 6,0 mmol/l, so sollte die RAASi in der Dosis passager reduziert oder pausiert werden. Schleifen- und Thiaziddiuretika können ebenso wie SGLT-2-Hemmer zur Senkung der [K+] eingesetzt werden, wenn primär bereits eine Indikation dafür besteht (Hypervolämie, Proteinurie etc.).
Ernährung
Es gelten dieselben diätologischen Überlegungen wie bei CKD.
Medikamente – RAASi
Für Patient:innen mit CKD, DM und HF konnte gezeigt werden, dass das Auftreten einer Hyperkaliämie der limitierende Faktor für eine maximal-intensive RAASi-Therapie ist [296]. Eine Beendigung der RAAS-Blockade verbessert zwar die [S‑K+], ist aber mit einem erhöhten kardiovaskulären Risiko bei Patient:innen mit HF oder CKD assoziiert [243, 297, 298]. Durch den Einsatz von intestinalen Kaliumbindern wie Patiromer kann die Hyperkaliämie in vielen Risikosituationen (CKD, HF, DM) effektiv behandelt werden, sodass die RAAS-Blockade deutlich seltener beendet werden muss [245‐247, 299‐301]. Eine ähnliche kaliumsenkende Wirkung kann auch mit SZC erreicht werden, die aktuelle Evidenz ist aber geringer als mit Patiromer [251, 302‐304]. Auch Real-Life-Daten haben gezeigt, dass mit SZC oder Patiromer in mehr als 80 % die RAASi-Therapie beibehalten werden konnte [302, 305]. Der Einsatz von Kaliumbindern sollte bei Risikopatient:innen ab einem [S‑K+] von > 5,5 mmol/l erwogenen werden. Es gilt wieder die oben erwähnte Einschränkung für SZC bezüglich der Entwicklung von Ödemen.
Aber auch begleitende Therapien mit Hydrochlorothiazid, Schleifendiuretika oder SGLT-2-Hemmern reduzieren das Hyperkaliämierisiko unter RAASi. Sie können, je nach Komorbiditäten (z. B. Diuretika bei Hypertonie oder HF), gezielt zur Kaliumsenkung eingesetzt werden [266, 306‐309]. Ob die „prophylaktische“ Gabe eines Kaliumbinders/Diuretikums bei Patient:innen mit [S‑K+] > 4,5–5,0 mmol/l vor Beginn einer RAASi einen klinischen Vorteil hinsichtlich Mortalität oder zumindest des Auftretens einer Hyperkaliämie ergibt, ist derzeit noch nicht geklärt.
Kommentar
Bei AKI und Hyperkaliämie ist ein passageres Absetzten der RAASi in der Akutphase sinnvoll [310].
Chronische Therapie der Hyperkaliämie bei Herzinsuffizienz
Es wird empfohlen, die Herzinsuffizienztherapie (RAASi, Betablocker, MRA) möglichst aufrechtzuerhalten. Liegt die [S‑K+] unter Ausschöpfung der kaliumsenkenden Therapie aber > 6,0 mmol/l, so sollte die RAASi in der Dosis reduziert oder abgesetzt werden. Natriumfreie Kaliumbinder (z. B. Patiromer) können bei Patient:innen unter RAASi + [S‑K+] > 5,5 mmol/l eingesetzt werden, v. a. um den Einsatz bzw. die maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen. SGLT-2-Hemmer können die [S‑K+] senken und sollten als Teil der Herzinsuffizienztherapie eingesetzt werden. Schleifen- und Thiaziddiuretika können zur Senkung der [K+] eingesetzt werden, wenn primär bereits eine Indikation dafür besteht (Hypervolämie …).
Ernährung
Es gelten dieselben diätologischen Empfehlungen wie bei CKD.
Medikamente – RAASi
Das Absetzen von RAASi sollte vermieden und deshalb sollten primär andere Maßnahmen zur Kaliumsenkung begonnen werden [311]. Sacubitril/Valsartan verringert das Risiko v. a. für schwere Hyperkaliämien bei gleichzeitiger Therapie mit MRA im Vergleich zu ACEi bzw. Valsartan [307, 312]. Eplerenon und Finerenon haben gegenüber Spironolacton den Vorteil einer kürzeren Halbwertszeit, was ggf. die Therapie der Hyperkaliämie erleichtert [32].
Kaliumbinder
In Effektivitätsstudien konnten sowohl Patiromer als auch SZC die [S‑K+] bei Patient:innen unter RAASi und MRA bei HFrEF senken [300, 313‐315]. Das primäre Ziel der Studien war es, die [S‑K+] in den Zielbereich zu senken (oder zu halten in PEARL-HF) und eine effektive RAAS-Blockade zu ermöglichen, was die Studien auch zum Teil zeigen konnten [316]. Aber der Effekt einer Kaliumbindertherapie auf die Einhaltung der Zieldosis einer RAAS-Blockade ist relativ klein [317]. Es existieren keine Studien, welche einen Mortalitätsvorteil durch eine medikamentöse Kaliumsenkung beweisen. In der REALIZE-K-Studie konnte trotz Optimierung des [S‑K+] mit SZC und der damit verbundenen effektiveren RAAS-Blockade ein möglicherweise negativer Effekt auf den kardiovaskulären Endpunkt (Tod oder Verschlechterung der HF) im Vergleich zu Placebo beobachtet werden (11 % vs. 3 %); die Studie war aber für diesen Endpunkt nicht ausgelegt. Eine potenzielle Ursache dafür war die Na+-Belastung durch SZC (Dosis 10–15 g/Tag) [314]. Das Risiko für Ödembildung, kardiale Dekompensationen und Mortalität war in einer retrospektiven Analyse mit SZC höher als mit Patiromer [204]. Eine entsprechende Warnung für die Verwendung von SZC bei Patient:innen mit Herzinsuffizienz wurde 2025 ausgegeben.
Eine Therapie mit Patiromer kann bei Patient:innen mit HF und einer [S‑K+] > 5,5–6,0 mmol/l empfohlen werden, um eine Therapie mit RAASi zu ermöglichen bzw. in den Dosiszielbereich zu bringen [318]. Sollte damit die [S‑K+] nicht < 5,1 mmol/l absinken, sollte die RAASi in der Dosis reduziert bzw. abgesetzt werden.
Diuretika
Schleifen- und Thiaziddiuretika führen zu einer effektiven Kaliumelimination, v. a. bei guter Nierenfunktion und können deshalb bei Patient:innen mit Hypervolämie und Hyperkaliämie eingesetzt werden [139, 319].
Bei Patient:innen mit HF unter einer MRA-Therapie sinkt das Hyperkaliämierisiko unter zusätzlicher Therapie mit SGLT2‑Hemmer um bis zu 50 % [265, 320, 321].
Positive Effekte auf die [S‑K+] wurden auch unter Vericiguat beobachtet [322].
Eine Puffertherapie bei metaboler Azidose mit NaHCO3 kann aufgrund der Na+-Belastung und des Risikos für einer Hypervolämie nicht empfohlen werden.
Chronische Therapie der Hyperkaliämie bei Diabetes
Es wird empfohlen, die kardio- und nephroprotektive Therapie mit RAASi bei Diabetes mellitus Typ 2 möglichst aufrechtzuerhalten. Liegt die [S‑K+] unter Ausschöpfung der kaliumsenkenden Therapie aber > 6,0 mmol/l, so sollte die RAASi in der Dosis reduziert oder abgesetzt werden. Kaliumbinder (Patiromer oder SZC) können bei Patient:innen unter RAASi + [S‑K+] > 5,5 mmol/l eingesetzt werden, v. a. um den Einsatz bzw. die maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen. SGLT-2-Hemmer können die [S‑K+] senken und sollten als Teil der Nephroprotektion bei Diabetes eingesetzt werden. Schleifen- und Thiaziddiuretika können zur Senkung der [K+] eingesetzt werden, wenn primär bereits eine Indikation dafür besteht (Hypervolämie, Hypertonie etc.).
Ernährung
Es wird wie bei CKD empfohlen, die Kaliumzufuhr zu evaluieren und bei hoher Kaliumzufuhr eine Einschränkung anzustreben. Eine geplante Studie bei DM vergleicht Diät vs. SZC könnte helfen, zukünftig diese Frage besser beantworten zu können [323].
Kaliumbinder
Patiromer senkt effektiv die [S‑K+] unter 5,0 mmol/l bei > 75 % der Patient:innen mit DM, CKD und Hyperkaliämie unter RAASi-Therapie [245]. Ähnliche positive Effekte konnte auch in der OPAL-HK-Studie, bei der ca. 50 % der Patient:innen mit DM eingeschlossen wurden, beobachtet werden [246]. Wirksam dürfte auch SZC sein, wie die HARMONIZE-Studie zeigte, bei der ca. 70 % der Patient:innen einen DM hatten [249]. In dieser Studie (viele Patient:innen mit CKD/HF/DM) wurde erstmals beobachtet, dass dosisabhängig, das Risiko für eine Ödembildung durch den Natriumgehalt von SZC steigt. Bei einer Tagesdosis von 5 g lag das Ödemrisiko mit 2,2 % auf Placeboniveau, bei 10 g bereits bei 5,9 % und bei 15 g immerhin bei 14,3 % [249].
SGLT-2-Hemmer
SGLT2‑Hemmer können das Hyperkaliämierisiko etwas reduzieren (Absinken der [S‑K+] um ca. 0,3 mmol/l). Dieser Effekt ist v. a. bei höheren [S‑K+] zu beobachten. Hypokaliämien werden unter SGLT-2‑Hemmer hingegen nicht beobachtet. Bei Patient:innen mit CKD und DM senkt eine vorbestehende Therapie mit SGLT-2‑Hemmer das Risiko, nach Einleitung einer ns-MRA-Therapie eine Hyperkaliämie zu entwickeln, signifikant [29]. Werden SGLT-2-Hemmer bei DM unter RAASi-Therapie eingesetzt, so ist das Hyperkaliämierisiko um ca. 10 % geringer [308]. Diese Beobachtung konnte in der prospektiven CONFIDENCE-Studie bestätigt werden, obwohl die Risikoreduktion für Hyperkaliämien ([S‑K+] 5,5–6,0 mmol/l) in der Gruppe mit Finerenon + Empagliflozin im Vergleich zu Finerenon alleine gering war (ca. 15–20 %; absolut: 13 vs. 16,7 %) [167]. Auch bei der Therapie mit Eplerenon reduziert die Kombination mit einem SGLT-2-Hemmer das Risiko einer Hyperkaliämie bei CKD und DM (17,4 % vs. 4,3 %) [265].
Therapie des hyporeninämischen Hypoaldosteronismus
Eine spezielle Situation bei Menschen mit Diabetes ist der hyporeninämische Hypoaldosteronismus: Diese Patient:innengruppe ist besonders gefährdet, unter einer RAASi eine Hyperkaliämie zu entwickeln. Neben der Therapie mit Kaliumbinder und Diät zeigen Thiaziddiuretika oder Schleifendiuretika eine gut kaliumsenkende Wirkung [324]. Auch eine Puffertherapie könnte die [S‑K+] positiv beeinflussen, aber die Azidose ist stark abhängig von der Hyperkaliämie, sodass eine effektive Senkung der [S‑K+] auch die Azidose verbessert [325]. Dies gründet darauf, dass eine Hyperkaliämie die renale Ammoniumproduktion/-elimination hemmt und damit die Säureeliminationskapazität verringert [79]. In einer älteren Studie wurde der Einsatz von Fludrocortison überprüft, welches ebenfalls zu einer Absenkung der [S‑K+] und einer Besserung der Azidose führt [326]. Aufgrund der meist notwendigen hohen Dosis von > 0,2 mg/Tag ist das Risiko für eine Ödembildung und Steigerung des Blutdrucks aber sehr hoch, sodass diese Therapie nur für Einzelfälle infrage kommt [159, 325].
Spezielle Therapiesituationen
Hypoaldosteronismus
Bei primärer Nebenniereninsuffizienz ist neben der Substitution von Cortisol auch die Gabe von Mineralokortikoiden notwendig; meistens sobald die Hydrocortisondosis < 50 mg/Tag beträgt (40 mg Hydrocortison hat eine mineralokortikoide Wirkung von 0,1 mg Fludrocortison) [327]. Die Fludrocortison-Startdosis liegt bei 0,05–0,1 mg/Tag und wird je nach Wirkung nach oben titriert. Bei isoliertem Hypoaldosteronismus ist die Therapie der Wahl ebenfalls Fludrocortison mit derselben Dosierung. Bezüglich des hyporeninämischen Hypoaldosteronismus s. Therapie des Diabetes.
Gordon-Syndrome (PHA II)
Aufgrund der Pathophysiologie mit einer Überstimulation des NaCl-Transporters am distalen Tubulus ist die Therapie mit Thiaziddiuretika das Mittel der Wahl, da diese direkt die Wirkung des Transporters inhibieren [328].
Pseudohypoaldosteronismus Typ 1
Während der Typ 1a im Erwachsenenalter einen milderen Phänotyp aufweist, der meistens keiner Therapie bedarf, ist beim PHA 1b eine lebenslange hoch dosierte Salzsubstitution (NaCl ca. 15–20 g/Tag und/oder NaHCO3 ca. 1 mmol/kg/Tag) gemeinsam mit einer Kaliumrestriktion (< 100 mmol/Tag) und einer hoch dosierten Kaliumbindertherapie notwendig. Die Dosis muss je nach Klinik und Labor (Na+, K+, HCO3−) angepasst werden [329].
Hyperkaliämie: Screening und Monitoring von Risikopatient:innen
- Bei oben genannten Risikopatient:innen (CKD, DM, HF) sollte im Rahmen der klinischen Routinekontrollen der Grunderkrankung und angepasst an den Schweregrad der chronischen Erkrankung (z. B. eGFR), aber mindestens 2 bis 4 mal/Jahr die [S‑K+] gemessen werden („Screening“). Gleichzeitig sollte auch die Nierenfunktion überprüft werden [156].
- Eine zusätzliche Kontrolle der [S‑K+] ist in dieser Patient:innengruppe auch bei jeder akut aufgetretenen Erkrankung (Fieber, Diarrhö etc.) empfehlenswert, ebenso in Situationen, die mit einem Abfall der GFR einhergehen können, sowie Verschlechterung der kardialen Situation oder Beginn einer Medikation, welche die [S‑K+] erhöhen könnte.
- Wird eine milde Hyperkaliämie festgestellt, so sollte innerhalb von 3 Tagen, bei moderater Hyperkaliämie innerhalb von 24 h, die [S‑K+] kontrolliert werden. Bei milder Hyperkaliämie mit unklarer Dynamik oder bei Patient:innen mit akuter Erkrankung (z. B. AKI, Rhabdomyolyse) ist aber eine kurzfristige Kontrolle (nach 1–2 h) erforderlich. Eine schwere Hyperkaliämie benötigt kurzfristigere Kontrollen und einen stationären Aufenthalt (s. schwere Hyperkaliämie).
- Die Kontrolle der [S‑K+] dient auch dazu, Hypokaliämien nach Einleitung einer kaliumsenkenden Maßnahme zu erkennen, obwohl das Risiko dafür eher gering ist (z. B. bei Kaliumbinder 2–10 %) [246, 249, 284, 300].
- Wird eine Episode einer Hyperkaliämie festgestellt und therapiert, so ist bei diesen Patient:innen das Risiko für weitere Episoden deutlich erhöht [140, 330, 331]. Deshalb sollten diese Patient:innen auch im Langzeitverlauf öfter kontrolliert werden.
- Es wird empfohlen, vor dem Beginn einer RAASi und 2 Wochen nach dem Start bzw. nach einer Dosiserhöhung eine Kontrolle der [S‑K+] durchzuführen [1, 156, 332]. Liegt die [S‑K+] > 4,5–5,0 mmol/l vor dem Therapiebeginn, so sollte die Therapie mit einem ACEi oder ARB, aber v. a. der Einsatz von MRA abgewogen werden bzw. entsprechend engmaschig kontrolliert werden. Die Anwendung von MRA bei einer [S‑K+] > 5 mmol/l und/oder eGFR < 30 ml/min/1,73 m2 sollte vermieden werden [156].
- Nach Absetzen einer RAASi-Therapie sollte die [S‑K+] nach spätestens einer Woche kontrolliert werden. Die Therapie mit einem Kaliumbinder sollte parallel dazu abgesetzt werden (oder in halber Dosis weitergeführt werden) [156].
- Auch wenn eine Hypokaliämie (bei Risikopatient:innen) mit oraler Kaliumsubstitution behandelt wird, sollten regelmäßig die [S‑K+] kontrolliert werden, um sog. posthypokaliämische Hyperkaliämien zu erkennen [333, 334].
Kommentar
Die Empfehlungen zur Kontrolle der [S‑K+] beschreiben nicht, wer (Hausarzt, Facharzt) die Kontrolle und Therapieanpassung veranlassen soll und wo (Krankenhausambulanz, niedergelassener Bereich) dies erfolgen soll, da diese von lokal unterschiedlich verfügbaren personellen und technischen Ressourcen (z. B. Blutgasanalysegeräte) abhängig ist. Es wird empfohlen, eine entsprechende Strategie, angepasst an die lokalen Gegebenheiten, zu entwickeln, um die Versorgung der Patient:innen zu ermöglichen. So sollte zum Beispiel eine Auslagerung der Kontrollen vom Krankenhaus in den niedergelassenen Bereich nur mit einer exakten Empfehlung zum Kontrollintervall und der Therapie erfolgen. Auch Geräte zur Selbstmessung der Kaliumwerte (ähnlich wie Blutzuckermessgeräte) könnten in Zukunft die Kontrolle von Risikopatient:innen unterstützen [335, 336].
Prävention der Hyperkaliämie
Die „sick day rules“ sollten den Patient:innen erklärt werden: Folgende Medikamente sollten bei Risikosituationen (Diarrhö, Fieber, schwere kardiale Dekompensation etc.) pausiert werden: ACEi, ARB, MRA, Aldosteronsynthasehemmer, (kaliumsparende) Diuretika; sowie unabhängig von einem Hyperkaliämierisiko: Metformin, SGLT2‑Hemmer. Diese kardio- und renoprotektiven Medikamente sollten nach der Stabilisierung der Patient:innen sobald wie möglich wieder begonnen werden [99]. Medikamente, mit Ausnahme der RAASi, welche eine Hyperkaliämie induzieren (NSAR, Trimethoprim, CNI), sollten bei Risikopatient:innen vermieden werden.
„Choosing wisely“ – Empfehlungen
Der prognostische Nutzen einer RAAS-modifizierenden Therapie (z. B. bei HF) bei hochbetagten oder multimorbiden Patient:innen ist ebenso limitiert wie der Einsatz von MRA bei Patient:innen mit einer eGFR < 30 ml/min/1,73 m2. Umgekehrt ist die Wahrscheinlichkeit der Nebenwirkungen einer RAAS-Hemmung (AKI, symptomatische Hypotonie, Stürze und Hyperkaliämie) in diesem Patient:innenkollektiv höher. In der Praxis stellen diese Patient:innen die mengenmäßig größte Gruppe dar, welche eine intensivmedizinische Behandlung wegen einer schweren Hyperkaliämie benötigen [337‐339]. Es sollte deshalb bei allen Patient:innen der zu erwartende Benefit einer RAASi-Therapie ebenso kritisch geprüft werden wie der Einsatz von Kaliumbinder. In der Praxis kann es gerechtfertigt sein, die RAASi-Therapie abzusetzen/nicht zu beginnen oder deutlich die entsprechenden Dosierungen zu reduzieren, um schwere Hyperkaliämien zu vermeiden.
Interessenkonflikt
M. Windpessl, M. Saemann, A. Kirsch, R. Edlinger: Vortragshonorare von Astra Zeneca und CSL Vifor. M. Pirklbauer: Reisekostenunterstützung und Vortragshonorare von Astra Zeneca und CSL Vifor. S.H. Ksiazek: Vortragshonorare von Astra Zeneca. G. Lindner und C. Schwarz geben an, dass kein Interessenkonflikt besteht.
Das Supplement finden Sie unter diesem Link.
Referenzen/Literatur
1.
Clase CM,Carrero J‑J, Ellison DH, Grams ME, Hemmelgarn BR, Jardine MJ, u. a. Potassium homeostasis andmanagement of dyskalemia in kidney diseases: conclusions from a Kidney Disease: Improving GlobalOutcomes (KDIGO) Controversies Conference. Kidney Int. 2020;97:42–61. https://doi.org/10.1016/j.kint.2019.09.018
2.
Cooper LB,Savarese G, Carrero J‑J, Szabo B, Jernberg T, Jonsson Å, u. a. Clinical and researchimplications of serum versus plasma potassium measurements. Eur J Heart Fail.2019;21:536–7. https://doi.org/10.1002/ejhf.1371
3.
StickleDF, Koob KR, McCudden CR. Characterizing ability of serum potassium (K)and the serum K reference interval to flag hypokalemia or hyperkalemia asobserved in plasma: A simulation study. Clin Biochem. 2023;118:110606. https://doi.org/10.1016/j.clinbiochem.2023.110606
4.
Lindner G,Burdmann EA, Clase CM, Hemmelgarn BR, Herzog CA, Małyszko J, u. a. Acute hyperkalemia in theemergency department: a summaryfrom a Kidney Disease: Improving GlobalOutcomes conference. Eur J Emerg Med Off J Eur Soc Emerg Med. 2020;27:329–37. https://doi.org/10.1097/MEJ.0000000000000691
5.
Varga C,Kálmán Z, Szakáll A, Drubits K, Koch M, Bánhegyi R, u. a. ECG alterations suggestive ofhyperkalemia in normokalemic versus hyperkalemic patients. BMC Emerg Med.2019;19:33. https://doi.org/10.1186/s12873-019-0247-0
6.
Raffee LA,Alawneh KZ, Ababneh MJ, Hijazi HH, Al Abdi RM, Aboozour MM, u. a. Clinical and electrocardiogrampresentations of patients with high serum potassium concentrations withinemergency settings: a prospective study. Int J Emerg Med.2022;15:23. https://doi.org/10.1186/s12245-022-00422-8
7.
Betts KA,Woolley JM, Mu F, McDonald E, Tang W, Wu EQ. The prevalence of hyperkalemia inthe United States. Curr Med Res Opin. 2018;34:971–8. https://doi.org/10.1080/03007995.2018.1433141
8.
Mu F,Betts KA, Woolley JM, Dua A, Wang Y, Zhong J, u. a. Prevalence and economic burden ofhyperkalemia in the United States Medicare population. Curr Med Res Opin.2020;36:1333–41. https://doi.org/10.1080/03007995.2020.1775072
9.
Singer AJ,Thode HC, Peacock WF. A retrospective study of emergency departmentpotassium disturbances: severity, treatment, and outcomes. Clin Exp Emerg Med.2017;4:73–9. https://doi.org/10.15441/ceem.16.194
10.
SarwarCMS, Papadimitriou L, Pitt B, Piña I, Zannad F, Anker SD, u. a. Hyperkalemia in Heart Failure. J Am Coll Cardiol. 2016;68:1575–89. https://doi.org/10.1016/j.jacc.2016.06.060
11.
Bandak G,Sang Y, Gasparini A, Chang AR, Ballew SH, Evans M, u. a. Hyperkalemia After InitiatingRenin-Angiotensin System Blockade: The Stockholm Creatinine Measurements(SCREAM) Project. J Am Heart Assoc. 2017;6:e005428. https://doi.org/10.1161/JAHA.116.005428
12.
Parikh RV,Nash DM, Brimble KS, Markle-Reid M, Tan TC, McArthur E, u. a. Kidney Function and PotassiumMonitoring After Initiation of Renin-Angiotensin-Aldosterone System BlockadeTherapy and Outcomes in 2 North American Populations. Circ Cardiovasc QualOutcomes. 2020;13:e006415. https://doi.org/10.1161/CIRCOUTCOMES.119.006415
13.
Marzano L,Merlo M, Martinelli N, Pizzolo F, Friso S. Efficacy and Safety of AldosteroneSynthase Inhibitors for Hypertension: A Meta-Analysis of RandomizedControlled Trials and Systematic Review. Hypertens Dallas Tex 1979.2025;82:e47–56. https://doi.org/10.1161/HYPERTENSIONAHA.124.23962
14.
Bakris GL,Saxena M, Gupta A, Chalhoub F, Lee J, Stiglitz D, u. a. RNA Interference With Zilebesiranfor Mild to Moderate Hypertension: The KARDIA‑1 Randomized Clinical Trial.JAMA. 2024;331:740–9. https://doi.org/10.1001/jama.2024.0728
15.
Desai AS,Karns AD, Badariene J, Aswad A, Neutel JM, Kazi F, u. a. Add-On Treatment With Zilebesiranfor Inadequately Controlled Hypertension: The KARDIA‑2 Randomized ClinicalTrial. JAMA. 2025;334:46–55. https://doi.org/10.1001/jama.2025.6681
16.
RheaultMN, Alpers CE, Barratt J, Bieler S, Canetta P, Chae D‑W, u. a. Sparsentan versus Irbesartan inFocal Segmental Glomerulosclerosis. N Engl J Med. Massachusetts MedicalSociety; 2023;389:2436–45. https://doi.org/10.1056/NEJMoa2308550
17.
Rovin BH,Barratt J, Heerspink HJL, Alpers CE, Bieler S, Chae D‑W, u. a. Efficacy and safety of sparsentanversus irbesartan in patients with IgA nephropathy (PROTECT): 2‑year resultsfrom a randomised, active-controlled, phase 3 trial. The Lancet. Elsevier; 2023;402:2077–90. https://doi.org/10.1016/S0140-6736(23)02302-4
18.
Parving H‑H,Brenner BM, McMurray JJV, de Zeeuw D, Haffner SM, Solomon SD, u. a. Cardiorenal end points in a trial of aliskiren for type 2 diabetes. N Engl J Med.2012;367:2204–13. https://doi.org/10.1056/NEJMoa1208799
19.
Hayes H,Russell R, Haugen A, Nagavally S, Sarvaideo J. The Utility of MonitoringPotassium in Transgender, Gender Diverse, and Nonbinary Individuals onSpironolactone. J Endocr Soc. 2022;6:bvac133. https://doi.org/10.1210/jendso/bvac133
20.
SOLVDInvestigators, Yusuf S, Pitt B, Davis CE, Hood WB, Cohn JN. Effect of enalaprilon survival in patients with reduced left ventricular ejection fractions andcongestive heart failure. N Engl J Med. 1991;325:293–302. https://doi.org/10.1056/NEJM199108013250501
21.
PfefferMA, Swedberg K, Granger CB, Held P, McMurray JJV, Michelson EL, u. a. Effects of candesartan onmortality and morbidity in patients with chronic heart failure: theCHARM-Overall programme. Lancet Lond Engl. 2003;362:759–66. https://doi.org/10.1016/s0140-6736(03)14282-1
22.
Weir MR,Rolfe M. Potassium homeostasis and renin-angiotensin-aldosterone systeminhibitors. Clin J Am Soc Nephrol CJASN. 2010;5:531–48. https://doi.org/10.2215/CJN.07821109
23.
ONTARGETInvestigators, Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, u. a. Telmisartan, ramipril, or both inpatients at high risk for vascular events. N Engl J Med. 2008;358:1547–59. https://doi.org/10.1056/NEJMoa0801317
24.
Zannad F,McMurray JJV, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, u. a. Eplerenone in patients withsystolic heart failure and mild symptoms. N Engl J Med. 2011;364:11–21. https://doi.org/10.1056/NEJMoa1009492
25.
WhitlockR, Leon SJ, Manacsa H, Askin N, Rigatto C, Fatoba ST, u. a. The association between dual RAASinhibition and risk of acute kidney injury and hyperkalemia in patients withdiabetic kidney disease: a systematicreview and meta-analysis. Nephrol Dial Transplant Off Publ Eur Dial TransplAssoc - Eur Ren Assoc. 2023;gfad101. https://doi.org/10.1093/ndt/gfad101
26.
Pitt B,Zannad F, Remme WJ, Cody R, Castaigne A, Perez A, u. a. The effect of spironolactone onmorbidity and mortality in patients with severe heart failure. RandomizedAldactone Evaluation Study Investigators. N Engl J Med. 1999;341:709–17. https://doi.org/10.1056/NEJM199909023411001
27.
Vardeny O,Wu DH, Desai A, Rossignol P, Zannad F, Pitt B, u. a. Influence of baseline andworsening renal function on efficacy of spironolactone in patients With severeheart failure: insights from RALES (Randomized Aldactone Evaluation Study). J Am Coll Cardiol. 2012;60:2082–9. https://doi.org/10.1016/j.jacc.2012.07.048
28.
Bakris GL,Ruilope LM, Anker SD, Filippatos G, Pitt B, Rossing P, u. a. A prespecified exploratory analysis from FIDELITY examined finerenone useand kidney outcomes in patients with chronic kidney disease and type 2 diabetes. Kidney Int. 2023;103:196–206. https://doi.org/10.1016/j.kint.2022.08.040
29.
Agarwal R,Joseph A, Anker SD, Filippatos G, Rossing P, Ruilope LM, u. a. Hyperkalemia Risk withFinerenone: Results from the FIDELIO-DKD Trial. J Am Soc Nephrol JASN. 2022;33:225–37. https://doi.org/10.1681/ASN.2021070942
30.
Idowu A,Lo KB, Adebolu O, Hamilton M, Abdelmaseeh P, Navaneethan SD, u. a. Hyperkalemia Risk of FinerenoneVersus Spironolactone in CKD patients with type 2 Diabetes. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc -Eur Ren Assoc. 2025;gfaf098. https://doi.org/10.1093/ndt/gfaf098
31.
Jhund PS,Talebi A, Henderson AD, Claggett BL, Vaduganathan M, Desai AS, u. a. Mineralocorticoid receptorantagonists in heart failure: an individual patient level meta-analysis. LancetLond Engl. 2024;404:1119–31. https://doi.org/10.1016/S0140-6736(24)01733-1
32.
Agarwal R,Pitt B, Palmer BF, Kovesdy CP, Burgess E, Filippatos G, u. a. A comparative post hoc analysis of finerenone and spironolactone inresistant hypertension in moderate-to-advanced chronic kidney disease. ClinKidney J. 2023;16:293–302. https://doi.org/10.1093/ckj/sfac234
33.
Wang C‑A,Lai H‑W, Chen J‑Y, Wang W‑J, Lin L‑C, Chiu Y‑L, u. a. Finerenone versus spironolactonein patients with chronic kidney disease and type 2 diabetes: a target trial emulation. Nat Commun.2025;16:9641. https://doi.org/10.1038/s41467-025-64640-3
34.
Floege J,Frankel AH, Erickson KF, Rtveladze K, Punekar Y, Mir JN, u. a. The burden of hyperkalaemia inchronic kidney disease: a systematicliterature review. Clin Kidney J. 2025;18:sfaf127. https://doi.org/10.1093/ckj/sfaf127
35.
WilliamsB, MacDonald TM, Morant S, Webb DJ, Sever P, McInnes G, u. a. Spironolactone versus placebo,bisoprolol, and doxazosin to determine the optimal treatment for drug-resistanthypertension (PATHWAY-2): a randomised,double-blind, crossover trial. Lancet Lond Engl. 2015;386:2059–68. https://doi.org/10.1016/S0140-6736(15)00257-3
36.
Fried LF,Emanuele N, Zhang JH, Brophy M, Conner TA, Duckworth W, u. a. Combined angiotensin inhibitionfor the treatment of diabetic nephropathy. N Engl J Med. 2013;369:1892–903. https://doi.org/10.1056/NEJMoa1303154
37.
FreemanMW, Halvorsen Y‑D, Marshall W, Pater M, Isaacsohn J, Pearce C, u. a. Phase 2 Trial of Baxdrostat for Treatment-Resistant Hypertension. N Engl JMed. 2023;388:395–405. https://doi.org/10.1056/NEJMoa2213169
38.
Massicotte-AzarniouchD, Canney M, Sood MM, Hundemer GL. Managing Hyperkalemia in the Modern Era:A Case-Based Approach. Kidney Int Rep. 2023;8:1290–300. https://doi.org/10.1016/j.ekir.2023.04.016
39.
Desai AS,Vaduganathan M, Claggett BL, Kulac IJ, Jhund PS, Cunningham J, u. a. Finerenone in Patients With a Recent Worsening Heart FailureEvent: The FINEARTS-HF Trial. J Am CollCardiol. 2025;85:106–16. https://doi.org/10.1016/j.jacc.2024.09.004
40.
Tuttle KR,Hauske SJ, Canziani ME, Caramori ML, Cherney D, Cronin L, u. a. Efficacy and safety ofaldosterone synthase inhibition with and without empagliflozin for chronickidney disease: a randomised, controlled, phase 2 trial. Lancet. 2024;403:379–90. https://doi.org/10.1016/S0140-6736(23)02408-X
41.
EdwardsNC, Steeds RP, Stewart PM, Ferro CJ, Townend JN. Effect of spironolactone onleft ventricular mass and aortic stiffness in early-stage chronic kidneydisease: a randomized controlled trial. J Am Coll Cardiol.2009;54:505–12. https://doi.org/10.1016/j.jacc.2009.03.066
42.
Pitt B,Pfeffer MA, Assmann SF, Boineau R, Anand IS, Claggett B, u. a. Spironolactone for heart failurewith preserved ejection fraction. N Engl J Med. 2014;370:1383–92. https://doi.org/10.1056/NEJMoa1313731
43.
Persson F,Lewis JB, Lewis EJ, Rossing P, Hollenberg NK, Parving H‑H, u. a. Impact of baseline renal functionon the efficacy and safety of aliskiren added to losartan in patients with type 2 diabetes and nephropathy. DiabetesCare. 2010;33:2304–9. https://doi.org/10.2337/dc10-0833
44.
SarafidisP, Agarwal R, Pitt B, Wanner C, Filippatos G, Boletis J, u. a. Outcomes with Finerenone inParticipants with Stage 4 CKD and Type 2 Diabetes: A FIDELITY Subgroup Analysis. Clin JAm Soc Nephrol. 2023;18:602–12. https://doi.org/10.2215/CJN.0000000000000149
45.
Ravioli S,Pluess E, Funk G‑C, Walter P, Schwarz C, Exadaktylos AK, u. a. Dyskalemias in patients withacute kidney injury presenting to the emergency department are common andindependent predictors of adverse outcome. Int J Clin Pract. 2021;75:e13653. https://doi.org/10.1111/ijcp.13653
46.
BachmannKF, Hess B, Koitmäe M, Bloch A, Regli A, Reintam Blaser A. Electrolytedisorders in the critically ill: a retrospective analysis. Sci Rep.2025;15:13943. https://doi.org/10.1038/s41598-025-98677-7
47.
ThomsenRW, Nicolaisen SK, Hasvold P, Sanchez RG, Pedersen L, Adelborg K, u. a. Elevated potassium levels inpatients with chronic kidney disease: occurrence, risk factors and clinicaloutcomes‑a Danish population-based cohort study. Nephrol Dial Transplant OffPubl Eur Dial Transpl Assoc - Eur Ren Assoc. 2018;33:1610–20. https://doi.org/10.1093/ndt/gfx312
48.
Lindner G, Pfortmüller CA, Leichtle AB, Fiedler GM,Exadaktylos AK. Age-relatedvariety in electrolyte levels and prevalence of dysnatremias and dyskalemias inpatients presenting to the emergency department. Gerontology. 2014;60:420–3. https://doi.org/10.1159/000360134
49.
ValdivielsoJM, Carriazo S, Martin M, Fernandez-Fernandez B, Bermudez-López M, Ortiz A, u. a. Gender-specific risk factors andoutcomes of hyperkalemia in CKD patients: smoking as a driver of hyperkalemia in men. Clin Kidney J. 2024;17:sfad212. https://doi.org/10.1093/ckj/sfad212
50.
Hougen I,Leon SJ, Whitlock R, Rigatto C, Komenda P, Bohm C, u. a. Hyperkalemia and its AssociationWith Mortality, Cardiovascular Events, Hospitalizations, and Intensive CareUnit Admissions in a Population-Based RetrospectiveCohort. Kidney Int Rep. 2021;6:1309–16. https://doi.org/10.1016/j.ekir.2021.02.038
51.
PfortmüllerCA, Leichtle AB, Fiedler GM, Exadaktylos AK, Lindner G. Hyperkalemia in theemergency department: etiology, symptoms and outcome of a life threateningelectrolyte disorder. Eur J Intern Med. 2013;24:e59-60. https://doi.org/10.1016/j.ejim.2013.02.010
52.
Sun J, LiuQ, Seery S, Sun L, Yuan Y, Wang W, u. a. The impact of hyperkalemia on ICU admissionand mortality: a retrospective study of Chineseemergency department data. BMC Emerg Med. 2024;24:95. https://doi.org/10.1186/s12873-024-01011-z
53.
ReinhardtM, Behnes M, Weidner K, Ayasse N, Lau F, Schmitt A, u. a. Potassium levels and short-termoutcomes in heart failure with mildly reduced ejection fraction. Int J Cardiol.2025;421:132878. https://doi.org/10.1016/j.ijcard.2024.132878
54.
CollinsAJ, Pitt B, Reaven N, Funk S, McGaughey K, Wilson D, u. a. Association of Serum Potassiumwith All-Cause Mortality in Patients with and without Heart Failure, ChronicKidney Disease, and/or Diabetes. Am J Nephrol. 2017;46:213–21. https://doi.org/10.1159/000479802
55.
Agiro A,Mu F, Cook E, Greatsinger A, Chen J, Zhao A, u. a. Hyperkalemia and the Risks ofAdverse Cardiovascular Outcomes in Patients With Chronic Kidney Disease. J Am Heart Assoc. 2025;14:e035256. https://doi.org/10.1161/JAHA.124.035256
56.
de RooijENM, de Fijter JW, Le Cessie S, Hoorn EJ, Jager KJ, Chesnaye NC, u. a. Serum Potassium and Risk of Deathor Kidney Replacement Therapy in Older People With CKD Stages 4‑5: Eight-YearFollow-up. Am J Kidney Dis Off J Natl Kidney Found. 2023;82:257–266.e1. https://doi.org/10.1053/j.ajkd.2023.03.008
57.
EinhornLM, Zhan M, Hsu VD, Walker LD, Moen MF, Seliger SL, u. a. The frequency of hyperkalemia andits significance in chronic kidney disease. Arch Intern Med. 2009;169:1156–62. https://doi.org/10.1001/archinternmed.2009.132
58.
GaspariniA, Evans M, Barany P, Xu H, Jernberg T, Ärnlöv J, u. a. Plasma potassium rangesassociated with mortality across stages of chronic kidney disease: theStockholm CREAtinine Measurements (SCREAM) project. Nephrol Dial Transplant OffPubl Eur Dial Transpl Assoc - Eur Ren Assoc. 2019;34:1534–41. https://doi.org/10.1093/ndt/gfy249
59.
KovesdyCP, Regidor DL, Mehrotra R, Jing J, McAllister CJ, Greenland S, u. a. Serum and dialysate potassiumconcentrations and survival in hemodialysis patients. Clin J Am Soc NephrolCJASN. 2007;2:999–1007. https://doi.org/10.2215/CJN.04451206
60.
KaraboyasA, Zee J, Brunelli SM, Usvyat LA, Weiner DE, Maddux FW, u. a. Dialysate Potassium, SerumPotassium, Mortality, and Arrhythmia Events in Hemodialysis: Results From theDialysis Outcomes and Practice Patterns Study (DOPPS). Am J Kidney Dis Off JNatl Kidney Found. 2017;69:266–77. https://doi.org/10.1053/j.ajkd.2016.09.015
61.
FerraroPM, Bolignano D, Aucella F, Brunori G, Gesualdo L, Limido A, u. a. Hyperkalemia excursions and riskof mortality and hospitalizations in hemodialysis patients: results fromDOPPS-Italy. J Nephrol. 2022;35:707–9. https://doi.org/10.1007/s40620-021-01209-5
62.
Bakris G,Agiro A, Mu F, Cook EE, Greatsinger A, Sundar M, u. a. Consequences of RecurrentHyperkalemia on Cardiovascular Outcomes and Mortality. JACC Adv. 2024;3:101331.https://doi.org/10.1016/j.jacadv.2024.101331
63.
TrevisanM, Clase CM, Evans M, Popov T, Ludvigsson JF, Sjölander A, u. a. Patterns of chronic and transienthyperkalaemia and clinically important outcomes in patients with chronic kidneydisease. Clin Kidney J. 2022;15:153–61. https://doi.org/10.1093/ckj/sfab159
64.
Gorriz JL,D’Marco L, Pastor-González A, Molina P, Gonzalez-Rico M, Puchades MJ, u. a. Long-term mortality andtrajectory of potassium measurements following an episode of acute severehyperkalaemia. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - EurRen Assoc. 2022;37:522–30. https://doi.org/10.1093/ndt/gfab003
65.
PrestonRA, Afshartous D, Rodco R, Alonso AB, Garg D. Evidence fora gastrointestinal-renal kaliuretic signaling axis in humans. Kidney Int.2015;88:1383–91. https://doi.org/10.1038/ki.2015.243
66.
Agarwal R,Afzalpurkar R, Fordtran JS. Pathophysiology of potassium absorption andsecretion by the human intestine. Gastroenterology. 1994;107:548–71. https://doi.org/10.1016/0016-5085(94)90184-8
67.
CeccantiC, Guidi L, D’Alessandro C, Cupisti A. Potassium Bioaccessibility in Uncookedand Cooked Plant Foods: Results from a Static In Vitro DigestionMethodology. Toxins. 2022;14:668. https://doi.org/10.3390/toxins14100668
68.
DeFronzoRA, Felig P, Ferrannini E, Wahren J. Effect of graded doses of insulin onsplanchnic and peripheral potassium metabolism in man. Am J Physiol.1980;238:E421-427. https://doi.org/10.1152/ajpendo.1980.238.5.E421
69.
Wouda RD,Gritter M, Karsten M, Michels EHA, Nieuweboer TM, Danser AHJ, u. a. Kaliuresis and IntracellularUptake of Potassium with Potassium Citrate and Potassium Chloride Supplements:A Randomized Controlled Trial. Clin JAm Soc Nephrol CJASN. 2023;18:1260–71. https://doi.org/10.2215/CJN.0000000000000228
70.
RabelinkTJ, Koomans HA, Hené RJ, Dorhout Mees EJ. Early and late adjustment topotassium loading in humans. Kidney Int. 1990;38:942–7. https://doi.org/10.1038/ki.1990.295
71.
Unwin RJ,Luft FC, Shirley DG. Pathophysiology and management of hypokalemia:a clinical perspective. Nat Rev Nephrol. 2011;7:75–84. https://doi.org/10.1038/nrneph.2010.175
72.
Epstein M, Lifschitz MD. The Unappreciated Role of Extrarenal and Gut Sensors in Modulating RenalPotassium Handling: Implications for Diagnosis of Dyskalemias and InterpretingClinical Trials. Kidney Int Rep. 2016;1:43–56. https://doi.org/10.1016/j.ekir.2016.03.001
73.
Grimm PR,Tatomir A, Rosenbaek LL, Kim BY, Li D, Delpire EJ, u. a. Dietary potassium stimulatesPpp1Ca-Ppp1r1a dephosphorylation of kidney NaCl cotransporter and reduces bloodpressure. J Clin Invest. 2023;133:e158498. https://doi.org/10.1172/JCI158498
74.
Palmer BF, Clegg DJ. Physiology and Pathophysiology of Potassium Homeostasis: Core Curriculum2019. Am J Kidney Dis Off J Natl Kidney Found. 2019;74:682–95. https://doi.org/10.1053/j.ajkd.2019.03.427
75.
WellingPA. Regulation of renal potassium secretion: molecular mechanisms. SeminNephrol. 2013;33:215–28. https://doi.org/10.1016/j.semnephrol.2013.04.002
76.
Al-QusairiL, Ferdaus MZ, Pham TD, Li D, Grimm PR, Zapf AM, u. a. Dietary anions control potassiumexcretion: it is more than a poorlyabsorbable anion effect. Am J Physiol Renal Physiol. 2023;325:F377–93. https://doi.org/10.1152/ajprenal.00193.2023
77.
HimathongkamT, Dluhy RG, Williams GH. Potassim-aldosterone-renin interrelationships.J Clin Endocrinol Metab. 1975;41:153–9. https://doi.org/10.1210/jcem-41-1-153
78.
Field MJ,Stanton BA, Giebisch GH. Influence of ADH on renal potassium handling:a micropuncture and microperfusion study. Kidney Int. 1984;25:502–11. https://doi.org/10.1038/ki.1984.46
79.
Harris AN,Grimm PR, Lee H‑W, Delpire E, Fang L, Verlander JW, u. a. Mechanism of Hyperkalemia-InducedMetabolic Acidosis. J Am Soc Nephrol JASN. 2018;29:1411–25. https://doi.org/10.1681/ASN.2017111163
80.
Palmer BF,Clegg DJ. Extrarenal Effects of Aldosterone on Potassium Homeostasis.Kidney360. 2022;3:561–8. https://doi.org/10.34067/KID.0006762021
81.
Choi HY,Ha SK. Potassium balances in maintenance hemodialysis. Electrolyte Blood PressE BP. 2013;11:9–16. https://doi.org/10.5049/EBP.2013.11.1.9
82.
Evers S, Engelien A, Karsch V, Hund M. Secondaryhyperkalaemic paralysis. J Neurol Neurosurg Psychiatry. 1998;64:249–52. https://doi.org/10.1136/jnnp.64.2.249
83.
KimmonsLA, Usery JB. Acute ascending muscle weakness secondary to medication-inducedhyperkalemia. Case Rep Med. 2014;2014:789529. https://doi.org/10.1155/2014/789529
84.
KarmacharyaP, Poudel DR, Pathak R, Rettew A, Alweis R. Acute hyperkalemia leading toflaccid paralysis: a review of hyperkalemic manifestations.J Community Hosp Intern Med Perspect. 2015;5:27993. https://doi.org/10.3402/jchimp.v5.27993
85.
Robert T,Mesnard L. How hyperkalemia affects the heart: clinical implications. NephrolDial Transplant Off Publ Eur Dial Transpl Assoc - Eur Ren Assoc.2025;40:1063–5. https://doi.org/10.1093/ndt/gfae287
86.
Mattu A,Brady WJ, Robinson DA. Electrocardiographic manifestations of hyperkalemia. AmJ Emerg Med. 2000;18:721–9. https://doi.org/10.1053/ajem.2000.7344
87.
Palmer BF,Clegg DJ. Hyperkalemia treatment standard. Nephrol Dial Transplant Off Publ EurDial Transpl Assoc - Eur Ren Assoc. 2024;39:1097–104. https://doi.org/10.1093/ndt/gfae056
88.
Parham WA, Mehdirad AA, Biermann KM, Fredman CS. Hyperkalemia revisited. Tex HeartInst J. 2006;33:40–7.
89.
LittmannL, Gibbs MA. Electrocardiographic manifestations of severe hyperkalemia.J Electrocardiol. 2018;51:814–7. https://doi.org/10.1016/j.jelectrocard.2018.06.018
90.
Weiss JN,Qu Z, Shivkumar K. Electrophysiology of Hypokalemia and Hyperkalemia. CircArrhythm Electrophysiol. 2017;10:e004667. https://doi.org/10.1161/CIRCEP.116.004667
91.
Ryuge A,Nomura A, Shimizu H, Fujita Y. Warning: The ECG May Be Normal in SevereHyperkalemia. Intern Med Tokyo Jpn. 2017;56:2243–4. https://doi.org/10.2169/internalmedicine.6895-15
92.
Varga C,Kálmán Z, Szakáll A, Drubits K, Koch M, Bánhegyi R, u. a. ECG alterations suggestive ofhyperkalemia in normokalemic versus hyperkalemic patients. BMC Emerg Med.2019;19:33. https://doi.org/10.1186/s12873-019-0247-0
93.
Ünlü L,Stephan F‑P, Riede FN, Mettler AC, Dutilh G, Capoferri G, u. a. Diagnostic accuracy of emergencydepartment ECGs in hyperkalemia detection: A cross-sectional study. Eur J Intern Med. 2025;136:56–62. https://doi.org/10.1016/j.ejim.2025.03.038
94.
MontagueBT, Ouellette JR, Buller GK. Retrospective review of the frequency of ECGchanges in hyperkalemia. Clin J Am Soc Nephrol CJASN. 2008;3:324–30. https://doi.org/10.2215/CJN.04611007
95.
Kim D,Jeong J, Kim J, Cho Y, Park I, Lee S‑M, u. a. Hyperkalemia Detection inEmergency Departments Using Initial ECGs: A Smartphone AI ECG Analyzer vs. Board-Certified Physicians. J Korean Med Sci. 2023;38:e322. https://doi.org/10.3346/jkms.2023.38.e322
96.
Xu D, ZhouB, Zhang J, Li C, Guan C, Liu Y, u. a. Prediction of hyperkalemia in ESRD patientsby identification of multiple leads and multiple features on ECG. Ren Fail.2023;45:2212800. https://doi.org/10.1080/0886022X.2023.2212800
97.
Pradhan J,Harding AM, Taylor SE, Lam Q. Implications of differences between point-of-careblood gas analyser and laboratory analyser potassium results on hyperkalaemiadiagnosis & treatment. Intern Med J. 2023;53:2035–41. https://doi.org/10.1111/imj.16020
98.
GhummanGM, Baqi A, Adil ANK, Khatri V. Role of point-of-care arterial blood potassiumin diagnosing pseudohyperkalemia. Proc Bayl Univ Med Cent. 2022;35:866–7. https://doi.org/10.1080/08998280.2022.2108979
99.
KidneyDisease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 ClinicalPractice Guideline for the Evaluation and Management of Chronic Kidney Disease.Kidney Int. 2024;105:S117–314. https://doi.org/10.1016/j.kint.2023.10.018
100.
Huth EJ,Squires RD, Elkinton JR. EXPERIMENTAL POTASSIUM DEPLETION IN NORMAL HUMANSUBJECTS. II. RENAL AND HORMONAL FACTORS IN THE DEVELOPMENT OF EXTRACELLULARALKALOSIS DURING DEPLETION. J Clin Invest. American Society for ClinicalInvestigation; 1959;38:1149–65. https://doi.org/10.1172/JCI103891
101.
HalperinML. Assessing the renal response in patients with potassium disorders:a shift in emphasis from the TTKG to the urine K+/creatinine ratio. Afr JNephrol. 2017;20:22–4. https://doi.org/10.21804/20-1-2453
102.
Hollander-RodriguezJC, Calvert JF. Hyperkalemia. Am Fam Physician. 2006;73:283–90.
103.
Dluhy RG,Axelrod L, Underwood RH, Williams GH. Studies of the control of plasmaaldosterone concentration in normal man. II. Effect of dietary potassium andacute potassium infusion. J Clin Invest. 1972;51:1950–7. https://doi.org/10.1172/JCI107001
104.
Ruiz-SánchezJG, Calle-Pascual AL, Rubio-Herrera MÁ, De Miguel Novoa MP, Gómez-Hoyos E,Runkle I. Clinical manifestations and associated factors in acquiredhypoaldosteronism in endocrinological practice. Front Endocrinol.2022;13:990148. https://doi.org/10.3389/fendo.2022.990148
105.
Arruda JA,Batlle DC, Sehy JT, Roseman MK, Baronowski RL, Kurtzman NA. Hyperkalemia andrenal insufficiency: role of selective aldosterone deficiency and tubularunresponsiveness to aldosterone. Am J Nephrol. 1981;1:160–7. https://doi.org/10.1159/000166533
106.
TakieddineLT, El-Khoury JM. Laboratory Anomalies in the Basic Metabolic Panel: CoreCurriculum 2025. Am J Kidney Dis Off J Natl Kidney Found. 2025;85:104–14. https://doi.org/10.1053/j.ajkd.2024.06.019
107.
Lano G,Lefevre F, Buffat C, Schlegel L, Dho E, Jantzen R, u. a. Pseudo-hyperkalaemia inambulatory samples: the never-ending story? Nephrol Dial Transplant Off PublEur Dial Transpl Assoc - Eur Ren Assoc. 2022;37:991–3. https://doi.org/10.1093/ndt/gfab355
108.
Saleh-AnarakiK, Jain A, Wilcox CS, Pourafshar N. Pseudohyperkalemia: Three Cases anda Review of Literature. Am J Med. 2022;135:e150–4. https://doi.org/10.1016/j.amjmed.2022.01.036
109.
Arani N, Wechsler AH. Hyperkalemia in the setting of severe leukocytosis: Should you treat? AmJ Emerg Med. 2023;66:174.e1-174.e2. https://doi.org/10.1016/j.ajem.2023.01.008
110.
Kalan U,Vardi J, Kaya SK, Gunes AK. A rare case of essential thrombocythemia withpseudo-hyperkalemia. Blood Coagul Fibrinolysis Int J Haemost Thromb.2024;35:214–6. https://doi.org/10.1097/MBC.0000000000001295
111.
FujimaruT, Hirose K, Yazawa M, Nagahama M, Kovesdy CP, Electrolyte Winter SeminarCollaborative Group. Pathophysiology and causes of hyperkalemia: unravelingcauses beyond kidney dysfunction. Clin Exp Nephrol. 2025; https://doi.org/10.1007/s10157-025-02711-x
112.
Kuwano K,Shimizu S, Fujita Y, Akatsu S, Shibagaki Y, Yazawa M. Marked hyperkalemia dueto inappropriate blood sample storage in two suspected cases of familialpseudohyperkalemia. CEN Case Rep. 2023;12:397–401. https://doi.org/10.1007/s13730-023-00781-y
113.
SennelsHP, Jørgensen HL, Goetze JP, Fahrenkrug J. Rhythmic 24-hour variations offrequently used clinical biochemical parameters in healthy young males--theBispebjerg study of diurnal variations. Scand J Clin Lab Invest.2012;72:287–95. https://doi.org/10.3109/00365513.2012.662281
114.
SchmidtST, Ditting T, Deutsch B, Schutte R, Friedrich S, Kistner I, u. a. Circadian rhythm and day to dayvariability of serum potassium concentration: a pilot study. J Nephrol. 2015;28:165–72. https://doi.org/10.1007/s40620-014-0115-7
115.
St-JulesDE, Clegg DJ, Palmer BF, Carrero J‑J. Can Novel Potassium Binders LiberatePeople with Chronic Kidney Disease from the Low-Potassium Diet?A Cautionary Tale. Clin J Am Soc Nephrol CJASN. 2022;17:467–72. https://doi.org/10.2215/CJN.09660721
116.
AronsonPS, Giebisch G. Effects of pH on potassium: new explanations for oldobservations. J Am Soc Nephrol JASN. 2011;22:1981–9. https://doi.org/10.1681/ASN.2011040414
117.
AronsonPS, Giebisch G. Effects of pH on potassium: new explanations for oldobservations. J Am Soc Nephrol JASN. 2011;22:1981–9. https://doi.org/10.1681/ASN.2011040414
118.
Sirken G,Raja R, Garces J, Bloom E, Fumo P. Contrast-induced translocationalhyponatremia and hyperkalemia in advanced kidney disease. Am J Kidney Dis Off JNatl Kidney Found. 2004;43:e31-35. https://doi.org/10.1053/j.ajkd.2003.10.028
119.
Jurkat-Rott K, Lehmann-Horn F. Genotype-phenotypecorrelation and therapeutic rationale in hyperkalemic periodic paralysis. Neurother J Am Soc Exp Neurother.2007;4:216–24. https://doi.org/10.1016/j.nurt.2007.02.001
120.
Karet FE.Mechanisms in hyperkalemic renal tubular acidosis. J Am Soc Nephrol JASN.2009;20:251–4. https://doi.org/10.1681/ASN.2008020166
121.
Adachi M,Motegi S, Nagahara K, Ochi A, Toyoda J, Mizuno K. Classification ofpseudohypoaldosteronism type II as type IV renal tubular acidosis:results of a literature review. Endocr J. 2023;70:723–9. https://doi.org/10.1507/endocrj.EJ22-0607
122.
Batlle DC, Arruda JA, Kurtzman NA. Hyperkalemic distal renal tubular acidosisassociated with obstructive uropathy. N Engl J Med. 1981;304:373–80. https://doi.org/10.1056/NEJM198102123040701
123.
Ravioli S,Woitok BK, Lindner G. BRASH syndrome - fact or fiction? A first analysisof the prevalence and relevance of a newly described syndrome. Eur J EmergMed Off J Eur Soc Emerg Med. 2021;28:153–5. https://doi.org/10.1097/MEJ.0000000000000762
124.
Yang M,White PC. Genetics and Pathophysiology of Classic Congenital AdrenalHyperplasia Due to 21-Hydroxylase Deficiency. J Clin Endocrinol Metab.2025;110:S1–12. https://doi.org/10.1210/clinem/dgae535
125.
Ruiz-SánchezJG, Calle-Pascual AL, Rubio-Herrera MÁ, De Miguel Novoa MP, Gómez-Hoyos E,Runkle I. Isolated hypoaldosteronism is a cause of hypovolemic but noteuvolemic hyponatremia. Endocr Connect. 2024;13:e230430. https://doi.org/10.1530/EC-23-0430
126.
NethatheGD, Lipman J, Anderson R, Feldman C. CIRMI‑a new term for a concept worthyof further exploration: a narrative review. Ann Transl Med. 2022;10:646. https://doi.org/10.21037/atm-21-5572
127.
Oster JR,Singer I, Fishman LM. Heparin-induced aldosterone suppression and hyperkalemia.Am J Med. 1995;98:575–86. https://doi.org/10.1016/s0002-9343(99)80017-5
128.
Laffin LJ,Rodman D, Luther JM, Vaidya A, Weir MR, Rajicic N, u. a. Aldosterone Synthase InhibitionWith Lorundrostat for Uncontrolled Hypertension: The Target-HTN RandomizedClinical Trial. JAMA. 2023;330:1140–50. https://doi.org/10.1001/jama.2023.16029
129.
Gupta N,Prasad P. Hyperkalemia in diabetes: newer insights into mechanism andtreatment. Postgrad Med J. 2022;98:e45. https://doi.org/10.1136/postgradmedj-2021-140226
130.
Hoorn EJ, Nelson JH, McCormick JA, Ellison DH. The WNK Kinase Network RegulatingSodium, Potassium, and Blood Pressure. J Am Soc Nephrol. 2011;22:605. https://doi.org/10.1681/ASN.2010080827
131.
Gordon RD,Geddes RA, Pawsey CG, O’Halloran MW. Hypertension and severe hyperkalaemiaassociated with suppression of renin and aldosterone and completely reversed bydietary sodium restriction. Australas Ann Med. 1970;19:287–94. https://doi.org/10.1111/imj.1970.19.4.287
132.
O’ShaughnessyKM. Gordon Syndrome: a continuing story. Pediatr Nephrol Berl Ger.2015;30:1903–8. https://doi.org/10.1007/s00467-014-2956-7
133.
Hoorn EJ,Walsh SB, McCormick JA, Fürstenberg A, Yang C‑L, Roeschel T, u. a. The calcineurin inhibitortacrolimus activates the renal sodium chloride cotransporter to causehypertension. Nat Med. 2011;17:1304–9. https://doi.org/10.1038/nm.2497
134.
Duan X‑P,Zhang C‑B, Wang W‑H, Lin D‑H. Role of calcineurin in regulating renal potassium(K+) excretion: Mechanisms of calcineurin inhibitor-induced hyperkalemia. ActaPhysiol Oxf Engl. 2024;240:e14189. https://doi.org/10.1111/apha.14189
135.
Rizk JG,Lazo JG, Quan D, Gabardi S, Rizk Y, Streja E, u. a. Mechanisms and management ofdrug-induced hyperkalemia in kidney transplant patients. Rev Endocr MetabDisord. 2021;22:1157–70. https://doi.org/10.1007/s11154-021-09677-7
136.
Smyrli M,Sarafidis PA, Loutradis C, Korogiannou M, Boletis IN, Marinaki S. Prevalenceand factors associated with hyperkalaemia in stable kidney transplantrecipients. Clin Kidney J. 2022;15:43–50. https://doi.org/10.1093/ckj/sfab129
137.
AdelborgK, Nicolaisen SK, Hasvold P, Palaka E, Pedersen L, Thomsen RW. Predictors forrepeated hyperkalemia and potassium trajectories in high-risk patients — Apopulation-based cohort study. PLOS ONE. Public Library of Science;2019;14:e0218739. https://doi.org/10.1371/journal.pone.0218739
138.
vanBoemmel-Wegmann S, Bauer C, Schuchhardt J, Hartenstein A, James G, Pessina E,u. a. HyperkalemiaIncidence in Patients With Non-Dialysis Chronic Kidney Disease: A Large Retrospective Cohort StudyFrom United States Clinical Care. Kidney Med. 2024;6:100879. https://doi.org/10.1016/j.xkme.2024.100879
139.
KreitzerN, Albert NM, Amin AN, Beavers CJ, Becker RC, Fonarow G, u. a. EMCREG-InternationalMultidisciplinary Consensus Panel on Management of Hyperkalemia in ChronicKidney Disease and Heart Failure. Cardiorenal Med. 2025;15:133–52. https://doi.org/10.1159/000543385
140.
Agiro A,Duling I, Eudicone J, Davis J, Brahmbhatt YG, Cooper K. The prevalence ofpredialysis hyperkalemia and associated characteristics among hemodialysispatients: The RE-UTILIZE study. Hemodial Int Int Symp Home Hemodial.2022;26:397–407. https://doi.org/10.1111/hdi.13006
141.
Yusuf AA,Hu Y, Singh B, Menoyo JA, Wetmore JB. Serum Potassium Levels and Mortality inHemodialysis Patients: A Retrospective Cohort Study. Am J Nephrol.2016;44:179–86. https://doi.org/10.1159/000448341
142.
Bleyer AJ,Hartman J, Brannon PC, Reeves-Daniel A, Satko SG, Russell G. Characteristics ofsudden death in hemodialysis patients. Kidney Int. 2006;69:2268–73. https://doi.org/10.1038/sj.ki.5000446
143.
Allon M,Takeshian A, Shanklin N. Effect of insulin-plus-glucose infusion with orwithout epinephrine on fasting hyperkalemia. Kidney Int. 1993;43:212–7. https://doi.org/10.1038/ki.1993.34
144.
Sumida K,Biruete A, Kistler BM, Khor B‑H, Ebrahim Z, Giannini R, u. a. New Insights Into DietaryApproaches to Potassium Management in Chronic Kidney Disease. J Ren Nutr Off J Counc Ren Nutr NatlKidney Found. 2023;33:S6–12. https://doi.org/10.1053/j.jrn.2022.12.003
145.
Bansal S,Pergola PE. Current Management of Hyperkalemia in Patients on Dialysis. KidneyInt Rep. 2020;5:779–89. https://doi.org/10.1016/j.ekir.2020.02.1028
146.
Walsh M,Collister D, Gallagher M, Mark PB, de Zoysa JR, Tyrwhitt J, u. a. Spironolactone versus placebo inpatients undergoing maintenance dialysis (ACHIEVE): an international,parallel-group, randomised controlled trial. Lancet Lond Engl. 2025;406:695–704. https://doi.org/10.1016/S0140-6736(25)01198-5
147.
Walsh M,Manns B, Garg AX, Bueti J, Rabbat C, Smyth A, u. a. The Safety of Eplerenone inHemodialysis Patients: A NoninferiorityRandomized Controlled Trial. Clin J Am Soc Nephrol CJASN. 2015;10:1602–8. https://doi.org/10.2215/CJN.12371214
148.
Sumida K,Yamagata K, Kovesdy CP. Constipation in CKD. Kidney Int Rep. 2020;5:121–34. https://doi.org/10.1016/j.ekir.2019.11.002
149.
GianneseD, D’Alessandro C, Pellegrino N, Panichi V, Cupisti A. RAASi Therapy Attenuatesthe Association between 24‑h Urinary Potassium Excretion and Dietary PotassiumIntake in CKD Patients. Nutrients. 2023;15:2454. https://doi.org/10.3390/nu15112454
150.
Roush GC,Ernst ME, Kostis JB, Yeasmin S, Sica DA. Dose doubling, relative potency, anddose equivalence of potassium-sparing diuretics affecting blood pressure andserum potassium: systematic review and meta-analyses. J Hypertens.2016;34:11–9. https://doi.org/10.1097/HJH.0000000000000762
151.
PerazellaMA. Trimethoprim-Induced Hyperkalaemia. Drug Saf. 2000;22:227–36. https://doi.org/10.2165/00002018-200022030-00006
152.
Baker M,Perazella MA. NSAIDs in CKD: Are They Safe? Am J Kidney Dis Off J Natl KidneyFound. 2020;76:546–57. https://doi.org/10.1053/j.ajkd.2020.03.023
153.
Nash DM,Markle-Reid M, Brimble KS, McArthur E, Roshanov PS, Fink JC, u. a. Nonsteroidal anti-inflammatorydrug use and risk of acute kidney injury and hyperkalemia in older adults: a population-based study. Nephrol DialTransplant Off Publ Eur Dial Transpl Assoc - Eur Ren Assoc. 2019;34:1145–54. https://doi.org/10.1093/ndt/gfz062
154.
Armstrong MJ, Zhang K, Ye F, Klarenbach SW, Pannu NI. Population-Based Analysis ofNonsteroidal Anti-inflammatory Drug Prescription in Subjects With ChronicKidney Disease. Can J Kidney Health Dis. 2023;10:20543581221149621. https://doi.org/10.1177/20543581221149621
155.
Ben SalemC, Badreddine A, Fathallah N, Slim R, Hmouda H. Drug-Induced Hyperkalemia. DrugSaf. 2014;37:677–92. https://doi.org/10.1007/s40264-014-0196-1
156.
Ngwenya B.UKKA Clinical Practice Guideline – Management of Hyperkalaemia in Adults –October 2023. 2023;
157.
JuurlinkDN, Mamdani MM, Lee DS, Kopp A, Austin PC, Laupacis A, u. a. Rates of hyperkalemia afterpublication of the Randomized Aldactone Evaluation Study. N Engl J Med.2004;351:543–51. https://doi.org/10.1056/NEJMoa040135
158.
EllisonDH, Terker AS, Gamba G. Potassium and Its Discontents: New Insight, NewTreatments. J Am Soc Nephrol JASN. 2016;27:981–9. https://doi.org/10.1681/ASN.2015070751
159.
Sousa AGP,Cabral JV de S, El-Feghaly WB, de Sousa LS, Nunes AB. Hyporeninemichypoaldosteronism and diabetes mellitus: Pathophysiology assumptions, clinicalaspects and implications for management. World J Diabetes. 2016;7:101–11. https://doi.org/10.4239/wjd.v7.i5.101
160.
Perez GO,Pelleya R, Oster JR, Kem DC, Vaamonde CA. Blunted kaliuresis after an acutepotassium load in patients with chronic renal failure. Kidney Int.1983;24:656–62. https://doi.org/10.1038/ki.1983.208
161.
Allon M,Dansby L, Shanklin N. Glucose modulation of the disposal of an acute potassiumload in patients with end-stage renal disease. Am J Med. 1993;94:475–82. https://doi.org/10.1016/0002-9343(93)90081-Y
162.
SchachterJ, Harper PH, Radin ME, Caggiula AW, McDonald RH, Diven WF. Comparison ofsodium and potassium intake with excretion. Hypertens Dallas Tex 1979.1980;2:695–9. https://doi.org/10.1161/01.hyp.2.5.695
163.
Tafesse E,Hurst M, Hoskin L, Badora K, Sugrue D, Qin L, u. a. Risk factors associated with theincidence and recurrence of hyperkalaemia in patients with cardiorenalconditions. Int J Clin Pract. 2021;75:e13941. https://doi.org/10.1111/ijcp.13941
164.
Bakris G,Agiro A, Mu F, Cook EE, Greatsinger A, Sundar M, u. a. Consequences of RecurrentHyperkalemia on Cardiovascular Outcomes and Mortality. JACC Adv. 2024;3:101331.https://doi.org/10.1016/j.jacadv.2024.101331
165.
MulkerrinE, Epstein FH, Clark BA. Aldosterone responses to hyperkalemia in healthyelderly humans. J Am Soc Nephrol JASN. 1995;6:1459–62. https://doi.org/10.1681/ASN.V651459
166.
KovesdyCP, Matsushita K, Sang Y, Brunskill NJ, Carrero JJ, Chodick G, u. a. Serum potassium and adverseoutcomes across the range of kidney function: a CKD Prognosis Consortium meta-analysis. Eur Heart J. 2018;39:1535–42. https://doi.org/10.1093/eurheartj/ehy100
167.
Agarwal R,Green JB, Heerspink HJL, Mann JFE, McGill JB, Mottl AK, u. a. Finerenone with Empagliflozin inChronic Kidney Disease and Type 2Diabetes. N Engl J Med. 2025; https://doi.org/10.1056/NEJMoa2410659
168.
FerreiraJP, Anker SD, Palmer BF, Pitt B, Rossing P, Ruilope LM, u. a. Incident hyperkalaemia risk modelin chronic kidney disease and diabetes: the FIDELITY programme. Eur Heart J.2025;ehaf258. https://doi.org/10.1093/eurheartj/ehaf258
169.
Xue C,Zhou C, Yang B, Ye X, Xu J, Lu Y, u. a. A Nomogramto Identify Hyperkalemia Risk in Patients with Advanced CKD. Kidney360.2022;3:1699–709. https://doi.org/10.34067/KID.0004752022
170.
SchoeberNHC, Linders M, Binkhorst M, De Boode W‑P, Draaisma JMT, Morsink M, u. a. Healthcare professionals’ knowledge of the systematic ABCDE approach: a cross-sectional study. BMC EmergMed. 2022;22:202. https://doi.org/10.1186/s12873-022-00753-y
171.
Cortés-OrtízA, Trujillo-Espinosa JA, Hernández-Lozada JA, Gracia-Ramos AE. Sinus arrestconsequence of moderate hyperkalemia: a case report. Oxf Med Case Rep.2025;2025:omaf059. https://doi.org/10.1093/omcr/omaf059
172.
Durfey N,Lehnhof B, Bergeson A, Durfey SNM, Leytin V, McAteer K, u. a. Severe Hyperkalemia: Can theElectrocardiogram Risk Stratify for Short-term Adverse Events? West J EmergMed. 2017;18:963–71. https://doi.org/10.5811/westjem.2017.6.33033
173.
Singer AJ,Thode HC, Peacock WF. Rapid correction of hyperkalemia is associated withreduced mortality in ED patients. Am J Emerg Med. 2020;38:2361–4. https://doi.org/10.1016/j.ajem.2019.12.012
174.
Lott C,Truhlář A, Alfonzo A, Barelli A, González-Salvado V, Hinkelbein J, u. a. European Resuscitation CouncilGuidelines 2021: Cardiac arrest in special circumstances. Resuscitation.2021;161:152–219. https://doi.org/10.1016/j.resuscitation.2021.02.011
175.
Piktel JS,Wan X, Kouk S, Laurita KR, Wilson LD. Beneficial Effect of Calcium Treatmentfor Hyperkalemia Is Not Due to “Membrane Stabilization”. Crit Care Med.2024;52:1499–508. https://doi.org/10.1097/CCM.0000000000006376
176.
Robert T,Joseph A, Mesnard L. Calcium salt during hyperkalemia. Kidney Int.2016;90:451–2. https://doi.org/10.1016/j.kint.2016.05.016
177.
Davey M,Caldicott D. Calcium salts in management of hyperkalaemia. Emerg Med J EMJ.2002;19:92–3. https://doi.org/10.1136/emj.19.1.92-a
178.
VandenHoek TL, Morrison LJ, Shuster M, Donnino M, Sinz E, Lavonas EJ, u. a. Part 12: cardiac arrest in special situations: 2010 American HeartAssociation Guidelines for Cardiopulmonary Resuscitation and EmergencyCardiovascular Care. Circulation. 2010;122:S829–861. https://doi.org/10.1161/CIRCULATIONAHA.110.971069
179.
CelebiYamanoglu NG, Yamanoglu A. The effect of calcium gluconate in the treatment ofhyperkalemia. Turk J Emerg Med. 2022;22:75–82. https://doi.org/10.4103/2452-2473.342812
180.
ZijlstraGJ. Challenging Dogma: Calcium Treatment in Hyperkalemia. Crit Care Med.2025;53:e760–1. https://doi.org/10.1097/CCM.0000000000006456
181.
EggertsenMA, Munch Johannsen C, Kovacevic A, Fink Vallentin M, Mørk Vammen L, AndersenLW, u. a. SodiumBicarbonate and Calcium Chloride for the Treatment of Hyperkalemia-InducedCardiac Arrest: A Randomized, Blinded,Placebo-Controlled Animal Study. Crit Care Med. 2024;52:e67–78. https://doi.org/10.1097/CCM.0000000000006089
182.
Hack JB,Woody JH, Lewis DE, Brewer K, Meggs WJ. The effect of calcium chloride intreating hyperkalemia due to acute digoxin toxicity in a porcine model.J Toxicol Clin Toxicol. 2004;42:337–42. https://doi.org/10.1081/clt-120039538
183.
VallentinMF, Povlsen AL, Granfeldt A, Terkelsen CJ, Andersen LW. Effect of calcium inpatients with pulseless electrical activity and electrocardiographiccharacteristics potentially associated with hyperkalemia and ischemia-sub-studyof the Calcium for Out-of-hospital Cardiac Arrest (COCA) trial. Resuscitation.2022;181:150–7. https://doi.org/10.1016/j.resuscitation.2022.11.006
184.
Jessen MK,Andersen LW, Djakow J, Chong NK, Stankovic N, Staehr C, u. a. Pharmacological interventions forthe acute treatment of hyperkalaemia: A systematic review and meta-analysis. Resuscitation. 2025;208:110489. https://doi.org/10.1016/j.resuscitation.2025.110489
185.
Allon M,Copkney C. Albuterol and insulin for treatment of hyperkalemia in hemodialysispatients. Kidney Int. 1990;38:869–72. https://doi.org/10.1038/ki.1990.284
186.
Harel Z,Kamel KS. Optimal Dose and Method of Administration of Intravenous Insulin inthe Management of Emergency Hyperkalemia: A Systematic Review. PloS One.2016;11:e0154963. https://doi.org/10.1371/journal.pone.0154963
187.
Dybdahl D,Roberson T, Rasor E, Kline L, Pershing M. Impact of a HyperkalemiaProtocol Tailored to Glucose Concentration and Renal Function onInsulin-Induced Hypoglycemia in Patients with Low Pretreatment Glucose.J Emerg Med. 2024;66:e421–31. https://doi.org/10.1016/j.jemermed.2023.12.001
188.
HumphreyTJL, James G, Wilkinson IB, Hiemstra TF. Clinical outcomes associated with theemergency treatment of hyperkalaemia with intravenous insulin-dextrose. Eur JIntern Med. 2022;95:87–92. https://doi.org/10.1016/j.ejim.2021.09.018
189.
Truhlář A,Deakin CD, Soar J, Khalifa GEA, Alfonzo A, Bierens JJLM, u. a. European Resuscitation CouncilGuidelines for Resuscitation 2015: Section 4. Cardiac arrest in special circumstances. Resuscitation. 2015;95:148–201. https://doi.org/10.1016/j.resuscitation.2015.07.017
190.
Robert T,Burbach M, Joseph A, Mesnard L. Sodium is the secret re-agent of bicarbonatetherapy during hyperkalemia. Kidney Int. 2016;90:450–1. https://doi.org/10.1016/j.kint.2016.05.015
191.
Joubert L,Radouco-Thomas C, Loiselle JM, Radouco-Thomas S, Turmel-Dorion L, Warren Y.A study in human pharmacology: evaluation of four diuretics anda placebo. Can Med Assoc J. 1968;99:57–63.
192.
Nguyen PT,Kataria VK, Sam TR, Hooper K, Mehta AN. Comparison of Patiromer to SodiumPolystyrene Sulfonate in Acute Hyperkalemia. Hosp Pharm. 2022;57:359–64. https://doi.org/10.1177/00185787211037552
193.
Grewal D,Urip L, Hong LT. Evaluation of Monotherapy Sodium Zirconium CyclosilicateVersus Sodium Polystyrene Sulfonate for Acute Hyperkalemia: A CohortStudy. Hosp Pharm. 2024;00185787241287676. https://doi.org/10.1177/00185787241287676
194.
Rydell A,Thackrey C, Molki M, Mullins BP. Effectiveness of Patiromer Versus SodiumZirconium Cyclosilicate for the Management of Acute Hyperkalemia. AnnPharmacother. 2024;58:790–5. https://doi.org/10.1177/10600280231209968
195.
Hagan AE,Farrington CA, Wall GC, Belz MM. Sodium polystyrene sulfonate for the treatmentof acute hyperkalemia: a retrospective study. Clin Nephrol. 2016;85:38–43.https://doi.org/10.5414/CN108628
196.
Rafique Z,Liu M, Staggers KA, Minard CG, Peacock WF. Patiromer for Treatment ofHyperkalemia in the Emergency Department: A Pilot Study. Acad Emerg MedOff J Soc Acad Emerg Med. 2020;27:54–60. https://doi.org/10.1111/acem.13868
197.
ShresthaDB, Budhathoki P, Sedhai YR, Baniya R, Cable CA, Kashiouris MG, u. a. Patiromer and Sodium ZirconiumCyclosilicate in Treatment of Hyperkalemia: A Systematic Review and Meta-Analysis. Curr Ther Res Clin Exp.2021;95:100635. https://doi.org/10.1016/j.curtheres.2021.100635
198.
KashiharaN, Kumeda Y, Higashino Y, Maeda Y, Kaneko Y, Kanai H, u. a. Efficacy and safety of patiromerfor non-dialysis and dialysis patients with hyperkalemia: the randomized,placebo-controlled and long-term study. Clin Exp Nephrol. 2025;29:548–59. https://doi.org/10.1007/s10157-024-02585-5
199.
Di PaloKE, Sinnett MJ, Goriacko P. Assessment of Patiromer Monotherapy forHyperkalemia in an Acute Care Setting. JAMA Netw Open. 2022;5:e2145236. https://doi.org/10.1001/jamanetworkopen.2021.45236
200.
RossignolP, Pitt B. Sodium polystyrene is unsafe and should not be prescribed for thetreatment of hyperkalaemia: primum non nocere! Clin Kidney J. 2023;16:1221–5. https://doi.org/10.1093/ckj/sfad090
201.
PeacockWF, Rafique Z, Vishnevskiy K, Michelson E, Vishneva E, Zvereva T, u. a. Emergency Potassium NormalizationTreatment Including Sodium Zirconium Cyclosilicate: A Phase II, Randomized, Double-blind,Placebo-controlled Study (ENERGIZE). Acad Emerg Med Off J Soc Acad Emerg Med.2020;27:475–86. https://doi.org/10.1111/acem.13954
202.
Cañas AE,Troutt HR, Jiang L, Tonthat S, Darwish O, Ferrey A, u. a. A randomized study to compare oral potassium binders in the treatment ofacute hyperkalemia. BMC Nephrol. 2023;24:89. https://doi.org/10.1186/s12882-023-03145-x
203.
Rafique Z,Budden J, Quinn CM, Duanmu Y, Safdar B, Bischof JJ, u. a. Patiromer utility as an adjuncttreatment in patients needing urgent hyperkalaemia management (PLATINUM):design of a multicentre, randomised,double-blind, placebo-controlled, parallel-group study. BMJ Open.2023;13:e071311. https://doi.org/10.1136/bmjopen-2022-071311
204.
Desai NR,Kammerer J, Budden J, Olopoenia A, Tysseling A, Gordon A. The Association ofHeart Failure and Edema Events between Patients Initiating Sodium ZirconiumCyclosilicate or Patiromer. Kidney360. 2024;5:1835–43. https://doi.org/10.34067/KID.0000000586
205.
Zhang Y,Xu R, Wang F, Liu Y, Xu J, Zhao N, u. a. Effects and Safety of a Novel Oral Potassium-LoweringDrug-Sodium Zirconium Cyclosilicate for the Treatment of Hyperkalemia: a Systematic Review and Meta-Analysis.Cardiovasc Drugs Ther. 2021;35:1057–66. https://doi.org/10.1007/s10557-020-07134-2
206.
NakayamaT, Kaneko H, Suzuki Y, Okada A, Morita H, Fujiu K, u. a. Sodium Polystyrene Sulfonate andHeart Failure Risk: A Comparative Study With CalciumPolystyrene Sulfonate. Nephrol Carlton Vic. 2025;30:e70117. https://doi.org/10.1111/nep.70117
207.
Zhuo M,Kim SC, Patorno E, Paik JM. Risk of Hospitalization for Heart Failure inPatients With Hyperkalemia Treated With Sodium Zirconium Cyclosilicate VersusPatiromer. J Card Fail. 2022;28:1414–23. https://doi.org/10.1016/j.cardfail.2022.04.003
208.
Amin AN,Menoyo J, Singh B, Kim CS. Efficacy and safety of sodium zirconiumcyclosilicate in patients with baseline serum potassium level ≥ 5.5 mmol/L: pooled analysis from two phase 3 trials. BMC Nephrol. 2019;20:440. https://doi.org/10.1186/s12882-019-1611-8
209.
Di PaloKE, Sinnett MJ, Goriacko P. Assessment of Patiromer Monotherapy forHyperkalemia in an Acute Care Setting. JAMA Netw Open. 2022;5:e2145236. https://doi.org/10.1001/jamanetworkopen.2021.45236
210.
Fravel MA,Meaney CJ, Noureddine L. Management of Hyperkalemia in Patients with ChronicKidney Disease Using Renin Angiotensin Aldosterone System Inhibitors. CurrHypertens Rep. 2023;25:395–404. https://doi.org/10.1007/s11906-023-01265-1
211.
ArampatzisS, Funk G‑C, Leichtle A, Fiedler G, Schwarz C, Zimmermann H, u. a. Impact of diuretictherapy-associated electrolyte disorders present on admission to the emergencydepartment: A cross-sectional analysis. BMCMed. 2013;11:83. https://doi.org/10.1186/1741-7015-11-83
212.
Te Dorsthorst RPM, Hendrikse J, Vervoorn MT, van WeperenVYH, van der Heyden MAG. Reviewof case reports on hyperkalemia induced by dietary intake: not restricted tochronic kidney disease patients. Eur J Clin Nutr. 2019;73:38–45. https://doi.org/10.1038/s41430-018-0154-6
213.
Lim CC,Tan NC, Teo EPS, Kadir HBA, Kwek JL, Bee YM, u. a. Non-Steroidal Anti-InflammatoryDrugs and Risk of Acute Kidney Injury and Hyperkalemia in Older Adults: A Retrospective Cohort Study andExternal Validation of a ClinicalRisk Model. Drugs Aging. 2022;39:75–82. https://doi.org/10.1007/s40266-021-00907-w
214.
Butterhoff MH, Derijks HJ, Hermens W, van der Linden PD. Sulfamethoxazole-Trimethoprim-InducedHyperkalemia in Hospitalized Patients Using Potassium-Sparing Drugs: AnObservational Study. Sr Care Pharm. 2024;39:259–66. https://doi.org/10.4140/TCP.n.2024.259
215.
NaseralallahL, Nasrallah D, Koraysh S, Aboelbaha S, Hussain TA. A Comparative StudyAssessing the Incidence and Degree of Hyperkalemia in Patients onUnfractionated Heparin versus Low-Molecular Weight Heparin. Clin Pharmacol AdvAppl. 2024;16:33–40. https://doi.org/10.2147/CPAA.S487288
216.
Hwang YJ,Muanda FT, McArthur E, Weir MA, Sontrop JM, Lam NN, u. a. Trimethoprim-sulfamethoxazole andthe risk of a hospital encounter withhyperkalemia: a matched population-based cohortstudy. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - Eur Ren Assoc.2023;38:1459–68. https://doi.org/10.1093/ndt/gfac282
217.
Pirklbauer M. Dialysevorschrift. Nephrol. 2023;18:131–7. https://doi.org/10.1007/s11560-023-00632-y
218.
PirklbauerM. Hemodialysis treatment in patients with severe electrolyte disorders:Management of hyperkalemia and hyponatremia. Hemodial Int Int Symp HomeHemodial. 2020;24:282–9. https://doi.org/10.1111/hdi.12845
219.
BlumbergA, Roser HW, Zehnder C, Müller-Brand J. Plasma potassium in patients withterminal renal failure during and after haemodialysis; relationship withdialytic potassium removal and total body potassium. Nephrol Dial TransplantOff Publ Eur Dial Transpl Assoc - Eur Ren Assoc. 1997;12:1629–34. https://doi.org/10.1093/ndt/12.8.1629
220.
Dépret F,Peacock WF, Liu KD, Rafique Z, Rossignol P, Legrand M. Management ofhyperkalemia in the acutely ill patient. Ann Intensive Care. 2019;9:32. https://doi.org/10.1186/s13613-019-0509-8
221.
Garg N,Kumar V, Sohal PM, Jain D, Jain A, Makkar V, u. a. Efficacy and Outcome ofIntermittent Peritoneal Dialysis in Patients with Acute Kidney Injury: A Single-Center Experience. Saudi JKidney Dis Transplant. 2020;31:423. https://doi.org/10.4103/1319-2442.284017
222.
Urgentinitiation of hemodialysis versus peritoneal dialysis in severe hyperkalemia:a prospective study | Clinical Kidney Journal | Oxford Academic[Internet]. [zitiert 29. November 2025]. https://academic.oup.com/ckj/advance-article/doi/10.1093/ckj/sfaf343/8316135.Zugegriffen 29 Nov 2025
223.
Houzé P,Baud FJ, Raphalen J‑H, Winchenne A, Moreira S, Gault P, u. a. Continuous renal replacementtherapy in the treatment of severe hyperkalemia: An in vitro study. Int J ArtifOrgans. SAGE Publications Ltd STM; 2020;43:87–93. https://doi.org/10.1177/0391398819865748
224.
Hirve AA,Repp AB, Burgess L‑AK. Things We Do for No ReasonTM: Obtaining anelectrocardiogram for managing mild hyperkalemia in hospitalized adults.J Hosp Med. 2024;19:841–4. https://doi.org/10.1002/jhm.13288
225.
MahoneyBA, Smith W a. D, Lo DS, Tsoi K, Tonelli M, Clase CM. Emergency interventionsfor hyperkalaemia. Cochrane Database Syst Rev. 2005;2005:CD003235. https://doi.org/10.1002/14651858.CD003235.pub2
226.
Dépret F,Peacock WF, Liu KD, Rafique Z, Rossignol P, Legrand M. Management ofhyperkalemia in the acutely ill patient. Ann Intensive Care. 2019;9:32. https://doi.org/10.1186/s13613-019-0509-8
227.
MontfordJR, Linas S. How Dangerous Is Hyperkalemia? J Am Soc Nephrol JASN.2017;28:3155–65. https://doi.org/10.1681/ASN.2016121344
228.
Obi Y,Thomas F, Dashputre AA, Goedecke P, Kovesdy CP. Long-term Patiromer Use andOutcomes Among US Veterans With Hyperkalemia and CKD: A Propensity-MatchedCohort Study. Kidney Med. 2024;6:100757. https://doi.org/10.1016/j.xkme.2023.100757
229.
Weir MR,Bakris GL, Gross C, Mayo MR, Garza D, Stasiv Y, u. a. Treatment with patiromerdecreases aldosterone in patients with chronic kidney disease and hyperkalemiaon renin-angiotensin system inhibitors. Kidney Int. 2016;90:696–704. https://doi.org/10.1016/j.kint.2016.04.019
230.
Ramos CI,González-Ortiz A, Espinosa-Cuevas A, Avesani CM, Carrero JJ, Cuppari L. Doesdietary potassium intake associate with hyperkalemia in patients with chronickidney disease? Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - EurRen Assoc. 2021;36:2049–57. https://doi.org/10.1093/ndt/gfaa232
231.
Bernier-JeanA, Wong G, Saglimbene V, Ruospo M, Palmer SC, Natale P, u. a. Dietary Potassium Intake andAll-Cause Mortality in Adults Treated with Hemodialysis. Clin J Am Soc NephrolCJASN. 2021;16:1851–61. https://doi.org/10.2215/CJN.08360621
232.
Tyson CC,Lin P‑H, Corsino L, Batch BC, Allen J, Sapp S, u. a. Short-term effects of the DASHdiet in adults with moderate chronic kidney disease: a pilot feeding study. Clin Kidney J. 2016;9:592–8. https://doi.org/10.1093/ckj/sfw046
233.
SaglimbeneVM, Wong G, Ruospo M, Palmer SC, Garcia-Larsen V, Natale P, u. a. Fruit and Vegetable Intake andMortality in Adults undergoing Maintenance Hemodialysis. Clin J Am Soc NephrolCJASN. 2019;14:250–60. https://doi.org/10.2215/CJN.08580718
234.
BorrelliS, De Nicola L, Minutolo R, Conte G, Chiodini P, Cupisti A, u. a. Current Management ofHyperkalemia in Non-Dialysis CKD: Longitudinal Study of Patients ReceivingStable Nephrology Care. Nutrients. 2021;13:942. https://doi.org/10.3390/nu13030942
235.
Turban S,Juraschek SP, Miller ER, Anderson CAM, White K, Charleston J, u. a. Randomized Trial on the Effectsof Dietary Potassium on Blood Pressure and Serum Potassium Levels in Adultswith Chronic Kidney Disease. Nutrients. 2021;13:2678. https://doi.org/10.3390/nu13082678
236.
Gritter M,Wouda RD, Yeung SMH, Wieërs MLA, Geurts F, de Ridder MAJ, u. a. Effects of Short-Term PotassiumChloride Supplementation in Patients with CKD. J Am Soc Nephrol JASN. 2022;33:1779–89. https://doi.org/10.1681/ASN.2022020147
237.
Rowan CG,Agiro A, Chan KA, Colman E, White K, Desai P, u. a. Hyperkalemia Recurrence FollowingMedical Nutrition Therapy in Patients with Stage 3‑4 Chronic Kidney Disease: The REVOLUTIONIZE I Real-World Study. AdvTher. 2024;41:2381–98. https://doi.org/10.1007/s12325-024-02835-8
238.
Goraya N,Simoni J, Jo C‑H, Wesson DE. A comparison of treating metabolic acidosisin CKD stage 4 hypertensive kidney disease with fruits and vegetables orsodium bicarbonate. Clin J Am Soc Nephrol CJASN. 2013;8:371–81. https://doi.org/10.2215/CJN.02430312
239.
Cupisti A,Kovesdy CP, D’Alessandro C, Kalantar-Zadeh K. Dietary Approach to Recurrent orChronic Hyperkalaemia in Patients with Decreased Kidney Function. Nutrients.2018;10:261. https://doi.org/10.3390/nu10030261
240.
Biruete A,Anderson C, Bernier-Jean A, Clase CM, Clegg D, Crews DC, u. a. ASN Kidney Health Guidance onPotassium and Phosphorus Food Additives. J Am Soc Nephrol JASN. 2025; https://doi.org/10.1681/ASN.0000000873
241.
Iman Y,Balshaw R, Alexiuk M, Hingwala J, Cahill L, Mollard R, u.a. Dietary potassiumliberalization with fruit and vegetables versus potassium restriction in peoplewith chronic kidney disease (DK-Lib CKD): a clinical trial protocol. BMCNephrol. 2023 24(1):301. doi: https://doi.org/10.1186/s12882-023-03354-4.
242.
An J, ZhouH, Ni L, Harrision TN, Wei R, Agiro A, u. a. Discontinuation ofRenin-Angiotensin-Aldosterone System Inhibitors Secondary to HyperkalemiaTranslates into Higher Cardiorenal Outcomes. Am J Nephrol. 2023;54:258–67. https://doi.org/10.1159/000531102
243.
Leon SJ,Whitlock R, Rigatto C, Komenda P, Bohm C, Sucha E, u. a. Hyperkalemia-RelatedDiscontinuation of Renin-Angiotensin-Aldosterone System Inhibitors and ClinicalOutcomes in CKD: A Population-Based Cohort Study. Am JKidney Dis Off J Natl Kidney Found. 2022;80:164–173.e1. https://doi.org/10.1053/j.ajkd.2022.01.002
244.
Li L,Harrison SD, Cope MJ, Park C, Lee L, Salaymeh F, u. a. Mechanism of Action andPharmacology of Patiromer, a NonabsorbedCross-Linked Polymer That Lowers Serum Potassium Concentration in Patients WithHyperkalemia. J Cardiovasc Pharmacol Ther.2016;21:456–65. https://doi.org/10.1177/1074248416629549
245.
Bakris GL,Pitt B, Weir MR, Freeman MW, Mayo MR, Garza D, u. a. Effect of Patiromer on SerumPotassium Level in Patients With Hyperkalemia and Diabetic Kidney Disease: TheAMETHYST-DN Randomized Clinical Trial. JAMA. 2015;314:151–61. https://doi.org/10.1001/jama.2015.7446
246.
Weir MR,Bakris GL, Bushinsky DA, Mayo MR, Garza D, Stasiv Y, u. a. Patiromer in patients with kidneydisease and hyperkalemia receiving RAAS inhibitors. N Engl J Med. 2015;372:211–21. https://doi.org/10.1056/NEJMoa1410853
247.
Agarwal R,Rossignol P, Romero A, Garza D, Mayo MR, Warren S, u. a. Patiromer versus placebo toenable spironolactone use in patients with resistant hypertension and chronickidney disease (AMBER): a phase 2, randomised, double-blind,placebo-controlled trial. Lancet Lond Engl. 2019;394:1540–50. https://doi.org/10.1016/S0140-6736(19)32135-X
248.
Roger SD,Lavin PT, Lerma EV, McCullough PA, Butler J, Spinowitz BS, u. a. Long-term safety and efficacy ofsodium zirconium cyclosilicate for hyperkalaemia in patients with mild/moderateversus severe/end-stage chronic kidney disease: comparative results from anopen-label, Phase 3 study. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - Eur RenAssoc. 2021;36:137–50. https://doi.org/10.1093/ndt/gfz285
249.
KosiborodM, Rasmussen HS, Lavin P, Qunibi WY, Spinowitz B, Packham D, u. a. Effect of Sodium ZirconiumCyclosilicate on Potassium Lowering for 28 Days Among Outpatients WithHyperkalemia: The HARMONIZE Randomized Clinical Trial. JAMA. 2014;312:2223–33. https://doi.org/10.1001/jama.2014.15688
250.
Zannad F,Hsu B‑G, Maeda Y, Shin SK, Vishneva EM, Rensfeldt M, u. a. Efficacy and safety of sodiumzirconium cyclosilicate for hyperkalaemia: the randomized, placebo-controlledHARMONIZE-Global study. ESC Heart Fail. 2020;7:55–65. https://doi.org/10.1002/ehf2.12561
251.
SpinowitzBS, Fishbane S, Pergola PE, Roger SD, Lerma EV, Butler J, u. a. Sodium Zirconium Cyclosilicateamong Individuals with Hyperkalemia: A 12-MonthPhase 3 Study. Clin J Am Soc Nephrol CJASN. 2019;14:798–809. https://doi.org/10.2215/CJN.12651018
252.
Ash SR,Batlle D, Kendrick J, Oluwatosin Y, Kooienga L, Eudicone JM, u. a. Sodium Zirconium Cyclosilicate inCKD, Hyperkalemia, and Metabolic Acidosis: NEUTRALIZE Randomized Study.Kidney360. 2024;5:812–20. https://doi.org/10.34067/KID.0000000000000446
253.
Lokelma |European Medicines Agency (EMA) [Internet]. 2018 [zitiert2. Oktober 2025]. https://www.ema.europa.eu/en/medicines/human/EPAR/lokelma.Zugegriffen 2 Okt 2025
254.
AvesaniCM, Heimbürger O, Rubin C, Sallstrom T, Fáxen-Irving G, Lindholm B, u. a. Plant-based diet in hyperkalemicchronic kidney disease patients receiving sodium zirconium cyclosilicate: a feasibility clinical trial. Am JClin Nutr. 2024;120:719–26. https://doi.org/10.1016/j.ajcnut.2024.06.025
255.
LaureatiP, Xu Y, Trevisan M, Schalin L, Mariani I, Bellocco R, u. a. Initiation of sodium polystyrenesulphonate and the risk of gastrointestinal adverse events in advanced chronickidney disease: a nationwide study. Nephrol DialTransplant Off Publ Eur Dial Transpl Assoc - Eur Ren Assoc. 2020;35:1518–26. https://doi.org/10.1093/ndt/gfz150
256.
RossignolP, Pitt B. Sodium polystyrene is unsafe and should not be prescribed for thetreatment of hyperkalaemia: primum non nocere! Clin Kidney J. 2023;16:1221–5. https://doi.org/10.1093/ckj/sfad090
257.
CarreroJJ, Sood MM, Gonzalez-Ortiz A, Clase CM. Pharmacological strategies to managehyperkalaemia: out with the old, in with the new? Not so fast…. Clin Kidney J.2023;16:1213–20. https://doi.org/10.1093/ckj/sfad089
258.
Jaques DA,Stucker F, Ernandez T, Alves C, Martin P‑Y, De Seigneux S, u. a. Comparative efficacy of patiromerand sodium polystyrene sulfonate on potassium levels in chronic haemodialysispatients: a randomized crossover trial. ClinKidney J. 2022;15:1908–14. https://doi.org/10.1093/ckj/sfac129
259.
Noel JA,Bota SE, Petrcich W, Garg AX, Carrero JJ, Harel Z, u. a. Risk of Hospitalization forSerious Adverse Gastrointestinal Events Associated With Sodium PolystyreneSulfonate Use in Patients of Advanced Age. JAMA Intern Med. 2019;179:1025–33. https://doi.org/10.1001/jamainternmed.2019.0631
260.
HolleckJL, Han L, Skanderson M, Bastian LA, Gunderson CG, Brandt CA, u. a. Risk of Serious AdverseGastrointestinal Events with Potassium Binders in Hospitalized Patients: A National Study. J Gen Intern Med. 2025;40:518–24. https://doi.org/10.1007/s11606-024-08979-1
261.
Palmer BF,Clegg DJ. Treatment of Abnormalities of Potassium Homeostasis in CKD. AdvChronic Kidney Dis. 2017;24:319–24. https://doi.org/10.1053/j.ackd.2017.06.001
262.
Agarwal R,Sinha AD, Cramer AE, Balmes-Fenwick M, Dickinson JH, Ouyang F, u. a. Chlorthalidone for Hypertensionin Advanced Chronic Kidney Disease. N Engl J Med. 2021;385:2507–19. https://doi.org/10.1056/NEJMoa2110730
263.
TrullàsJC, Morales-Rull JL, Casado J, Carrera-Izquierdo M, Sánchez-Marteles M,Conde-Martel A, u. a. Combining loop and thiazide diuretics for acute heart failure acrossthe estimated glomerular filtration rate spectrum: a post-hoc analysis of the CLOROTIC trial. Eur J Heart Fail. 2023; https://doi.org/10.1002/ejhf.2988
264.
EllisonDH. Clinical Pharmacology in Diuretic Use. Clin J Am Soc Nephrol CJASN.2019;14:1248–57. https://doi.org/10.2215/CJN.09630818
265.
ProvenzanoM, Jongs N, Vart P, Stefánsson BV, Chertow GM, Langkilde AM, u. a. The Kidney Protective Effects ofthe Sodium-Glucose Cotransporter‑2 Inhibitor, Dapagliflozin, Are Present inPatients With CKD Treated With Mineralocorticoid Receptor Antagonists. KidneyInt Rep. 2022;7:436–43. https://doi.org/10.1016/j.ekir.2021.12.013
266.
Neuen BL,Oshima M, Agarwal R, Arnott C, Cherney DZ, Edwards R, u. a. Sodium-Glucose Cotransporter 2Inhibitors and Risk of Hyperkalemia in People With Type 2 Diabetes: A Meta-Analysis of IndividualParticipant Data From Randomized, Controlled Trials. Circulation. AmericanHeart Association; 2022;145:1460–70. https://doi.org/10.1161/CIRCULATIONAHA.121.057736
267.
CharlwoodC, Chudasama J, Darling AL, Logan Ellis H, Whyte MB. Effect of sodium-glucoseco-transporter 2 inhibitors on plasma potassium: A meta-analysis.Diabetes Res Clin Pract. 2023;196:110239. https://doi.org/10.1016/j.diabres.2023.110239
268.
Albakr RB,Sridhar VS, Cherney DZI. Novel Therapies in Diabetic Kidney Disease and Risk ofHyperkalemia: A Review of the Evidence From Clinical Trials. Am J KidneyDis Off J Natl Kidney Found. 2023;82:737–42. https://doi.org/10.1053/j.ajkd.2023.04.015
269.
Sumida K,Dashputre AA, Potukuchi PK, Thomas F, Obi Y, Molnar MZ, u. a. Laxative Use and Risk ofDyskalemia in Patients with Advanced CKD Transitioning to Dialysis. J Am Soc Nephrol JASN. 2021;32:950–9. https://doi.org/10.1681/ASN.2020081120
270.
deBrito-Ashurst I, Varagunam M, Raftery MJ, Yaqoob MM. BicarbonateSupplementation Slows Progression of CKD and Improves Nutritional Status.J Am Soc Nephrol JASN. 2009;20:2075–84. https://doi.org/10.1681/ASN.2008111205
271.
BiCARBstudy group. Clinical and cost-effectiveness of oral sodium bicarbonate therapyfor older patients with chronic kidney disease and low-grade acidosis (BiCARB):a pragmatic randomised, double-blind, placebo-controlled trial. BMC Med.2020;18:91. https://doi.org/10.1186/s12916-020-01542-9
272.
Shi H, SuX, Yan B, Li C, Wang L. Effects of oral alkali drug therapy on clinicaloutcomes in pre-dialysis chronic kidney disease patients: a systematicreview and meta-analysis. Ren Fail. 2022;44:106–15. https://doi.org/10.1080/0886022X.2021.2023023
273.
Pun PH,Middleton JP. Dialysate Potassium, Dialysate Magnesium, and Hemodialysis Risk.J Am Soc Nephrol JASN. 2017;28:3441–51. https://doi.org/10.1681/ASN.2017060640
274.
Musso CG.Potassium metabolism in patients with chronic kidney disease. Part II:Patients on dialysis (stage 5). Int Urol Nephrol. 2004;36:469–72. https://doi.org/10.1007/s11255-004-6194-y
275.
Elliott AB, Soliman KMM, Ullian ME. Hyperkalemia in chronic peritoneal dialysispatients. Ren Fail. 2022;44:217–23. https://doi.org/10.1080/0886022X.2022.2032151
276.
Fa G, Jsde J, L C, Mct P, Lkrp de A, C SWM, u. a. Hypokalemia and hyperkalemia in patients onperitoneal dialysis: incidence and associated factors. Int Urol Nephrol[Internet]. Int Urol Nephrol; 2020 [zitiert 25. Juli 2025];52. https://doi.org/10.1007/s11255-020-02385-2
277.
Santoro A,Mancini E, London G, Mercadal L, Fessy H, Perrone B, u. a. Patients with complex arrhythmiasduring and after haemodialysis suffer from different regimens of potassiumremoval. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - Eur RenAssoc. 2008;23:1415–21. https://doi.org/10.1093/ndt/gfm730
278.
LabriolaL, Jadoul M. Sailing between Scylla and Charybdis: the high serum K‑lowdialysate K quandary. Semin Dial. 2014;27:463–71. https://doi.org/10.1111/sdi.12252
279.
Abuelo JG.Treatment of Severe Hyperkalemia: Confronting 4 Fallacies. Kidney Int Rep.2018;3:47–55. https://doi.org/10.1016/j.ekir.2017.10.001
280.
CharytanDM, Winkelmayer WC, Granger CB, Middleton JP, Herzog CA, Chertow GM, u. a. Effects of dialysate potassiumconcentration of 3.0 mmol/l with sodium zirconium cyclosilicate on dialysis-free days versusdialysate potassium concentration of 2.0 mmol/l alone on rates of cardiacarrhythmias in hemodialysis patients with hyperkalemia. Kidney Int.2025;107:169–79. https://doi.org/10.1016/j.kint.2024.10.010
281.
St-JulesDE, Goldfarb DS, Sevick MA. Nutrient Non-equivalence: Does RestrictingHigh-Potassium Plant Foods Help to Prevent Hyperkalemia in HemodialysisPatients? J Ren Nutr Off J Counc Ren Nutr Natl Kidney Found.2016;26:282–7. https://doi.org/10.1053/j.jrn.2016.02.005
282.
Noori N,Kalantar-Zadeh K, Kovesdy CP, Murali SB, Bross R, Nissenson AR, u. a. Dietary potassium intake andmortality in long-term hemodialysis patients. Am J Kidney Dis Off J Natl KidneyFound. 2010;56:338–47. https://doi.org/10.1053/j.ajkd.2010.03.022
283.
Arnold R,Pianta TJ, Pussell BA, Kirby A, O’Brien K, Sullivan K, u. a. Randomized, Controlled Trial ofthe Effect of Dietary Potassium Restriction on Nerve Function in CKD. Clin J AmSoc Nephrol CJASN. 2017;12:1569–77. https://doi.org/10.2215/CJN.00670117
284.
FishbaneS, Ford M, Fukagawa M, McCafferty K, Rastogi A, Spinowitz B, u. a. A Phase 3b, Randomized, Double-Blind,Placebo-Controlled Study of Sodium Zirconium Cyclosilicate for Reducing theIncidence of Predialysis Hyperkalemia. J Am Soc Nephrol JASN. 2019;30:1723–33. https://doi.org/10.1681/ASN.2019050450
285.
Ng JK‑C,Fung WW‑S, Chan GC‑K, Chow K‑M, Szeto C‑C. Intermittent sodium zirconiumcyclosilicate for the prevention of hyperkalemia in chronic kidney disease. BMCNephrol. 2025;26:260. https://doi.org/10.1186/s12882-025-04194-0
286.
FishbaneS, Dember LM, Jadoul M, Kovesdy CP, Guzman N, Kordzakhia G, u. a. The randomized DIALIZE-Outcomestrial evaluated sodium zirconium cyclosilicate in hemodialysis. Kidney Int.2025;S0085–2538(25)00509‑5. https://doi.org/10.1016/j.kint.2025.06.016
287.
MiddletonJP, Sun S, Murray S, Davenport CA, Daubert JP. Randomized Trial of Patiromer onEfficacy to Reduce Episodic Hyperkalemia in Patients with ESKD Treated WithHemodialysis. Kidney Int Rep. 2024;9:3218–25. https://doi.org/10.1016/j.ekir.2024.08.005
288.
KovesdyCP, Rowan CG, Conrad A, Spiegel DM, Fogli J, Oestreicher N, u. a. Real-World Evaluation ofPatiromer for the Treatment of Hyperkalemia in Hemodialysis Patients. KidneyInt Rep. 2019;4:301–9. https://doi.org/10.1016/j.ekir.2018.10.020
289.
MathialahanT, Sandle GI. Dietary potassium and laxatives as regulators of colonicpotassium secretion in end-stage renal disease. Nephrol Dial Transplant.2003;18:341–7. https://doi.org/10.1093/ndt/18.2.341
290.
Nata N,Bunpeth W, Tasanavipas P, Varothai N, Supasyndh O, Satirapoj B. Effect of sennaglycoside on serum potassium levels among patients on maintenance hemodialysis:A randomized controlled trial. Ther Apher Dial. 2022;26:908–14. https://doi.org/10.1111/1744-9987.13774
291.
Sibbel S,Walker AG, Colson C, Tentori F, Brunelli SM, Flythe J. Association ofContinuation of Loop Diuretics at Hemodialysis Initiation with ClinicalOutcomes. Clin J Am Soc Nephrol. 2019;14:95. https://doi.org/10.2215/CJN.05080418
292.
Bragg-GreshamJL, Fissell RB, Mason NA, Bailie GR, Gillespie BW, Wizemann V, u. a. Diuretic Use, Residual RenalFunction, and Mortality Among Hemodialysis Patients in the Dialysis Outcomesand Practice Pattern Study (DOPPS). Am J Kidney Dis. 2007;49:426–31. https://doi.org/10.1053/j.ajkd.2006.12.012
293.
SchambelanM, Sebastian A, Biglieri EG, Brust NL, Chang BC, Hirai J, u. a. Prevalence, pathogenesis, andfunctional significance of aldosterone deficiency in hyperkalemic patients withchronic renal insufficiency. Kidney Int. 1980;17:89–101. https://doi.org/10.1038/ki.1980.11
294.
Kaisar MO,Wiggins KJ, Sturtevant JM, Hawley CM, Campbell SB, Isbel NM, u. a. A randomized controlled trial of fludrocortisone for the treatment ofhyperkalemia in hemodialysis patients. Am J Kidney Dis Off J Natl Kidney Found.2006;47:809–14. https://doi.org/10.1053/j.ajkd.2006.01.014
295.
Allon M.Hyperkalemia in end-stage renal disease: mechanisms and management. J AmSoc Nephrol JASN. 1995;6:1134–42. https://doi.org/10.1681/ASN.V641134
296.
Epstein M.Hyperkalemia constitutes a constraint for implementingrenin-angiotensin-aldosterone inhibition: the widening gap between mandatedtreatment guidelines and the real-world clinical arena. Kidney Int Suppl.2016;6:20–8. https://doi.org/10.1016/j.kisu.2016.01.004
297.
TrevisanM, Fu EL, Xu Y, Savarese G, Dekker FW, Lund LH, u. a. Stopping mineralocorticoidreceptor antagonists after hyperkalaemia: trial emulation in data from routinecare. Eur J Heart Fail. 2021;23:1698–707. https://doi.org/10.1002/ejhf.2287
298.
Fu EL,Evans M, Clase CM, Tomlinson LA, van Diepen M, Dekker FW, u. a. Stopping Renin-Angiotensin SystemInhibitors in Patients with Advanced CKD and Risk of Adverse Outcomes: A Nationwide Study. J Am Soc Nephrol JASN. 2021;32:424–35. https://doi.org/10.1681/ASN.2020050682
299.
Pitt B,Anker SD, Lund LH, Coats AJS, Filippatos G, Rossignol P, u. a. Patiromer Facilitates AngiotensinInhibitor and Mineralocorticoid Antagonist Therapies in Patients With HeartFailure and Hyperkalemia. J Am CollCardiol. 2024;84:1295–308. https://doi.org/10.1016/j.jacc.2024.05.079
300.
Pitt B,Anker SD, Bushinsky DA, Kitzman DW, Zannad F, Huang I‑Z, u. a. Evaluation of the efficacy andsafety of RLY5016, a polymeric potassium binder, in a double-blind, placebo-controlledstudy in patients with chronic heart failure (the PEARL-HF) trial. Eur Heart J.2011;32:820–8. https://doi.org/10.1093/eurheartj/ehq502
301.
Agarwal R,Rossignol P, Mayo MR, Conrad A, Arthur S, Williams B, u. a. Patiromer to EnableSpironolactone in Patients with Resistant Hypertension and CKD (AMBER): Resultsin the Prespecified Subgroup with Diabetes. Clin J Am Soc Nephrol CJASN.2021;16:1407–9. https://doi.org/10.2215/CJN.02890221
302.
Agiro A,An A, Cook EE, Mu F, Chen J, Desai P, u. a. Real-World Modifications ofRenin-Angiotensin-Aldosterone System Inhibitors in Patients with HyperkalemiaInitiating Sodium Zirconium Cyclosilicate Therapy: The OPTIMIZE I Study. AdvTher. 2023;40:2886–901. https://doi.org/10.1007/s12325-023-02518-w
303.
Agiro A,Greatsinger A, Mu F, Cook EE, Chen J, Sundar M, u. a. Renin-Angiotensin-AldosteroneSystem Inhibitor Dosing After Initiation of Outpatient Sodium ZirconiumCyclosilicate Therapy: The GALVANIZE RAASi Real-World Evidence Study. Adv Ther.2025; https://doi.org/10.1007/s12325-025-03254-z
304.
Ash SR,Singh B, Lavin PT, Stavros F, Rasmussen HS. A phase 2 study onthe treatment of hyperkalemia in patients with chronic kidney disease suggeststhat the selective potassium trap, ZS‑9, is safe and efficient. Kidney Int.2015;88:404–11. https://doi.org/10.1038/ki.2014.382
305.
KovesdyCP, Gosmanova EO, Woods SD, Fogli JJ, Rowan CG, Hansen JL, u. a. Real-world management ofhyperkalemia with patiromer among United States Veterans. Postgrad Med.2020;132:176–83. https://doi.org/10.1080/00325481.2019.1706920
306.
ReardonLC, Macpherson DS. Hyperkalemia in outpatients using angiotensin-convertingenzyme inhibitors. How much should we worry? Arch Intern Med. 1998;158:26–32. https://doi.org/10.1001/archinte.158.1.26
307.
Desai AS,Vardeny O, Claggett B, McMurray JJV, Packer M, Swedberg K, u. a. Reduced Risk of HyperkalemiaDuring Treatment of Heart Failure With Mineralocorticoid Receptor Antagonistsby Use of Sacubitril/Valsartan Compared With Enalapril: A Secondary Analysis of thePARADIGM-HF Trial. JAMA Cardiol. 2017;2:79–85. https://doi.org/10.1001/jamacardio.2016.4733
308.
Wing S,Ray JG, Yau K, Jeyakumar N, Abdullah S, Luo B, u. a. SGLT2 Inhibitors and Risk forHyperkalemia Among Individuals Receiving RAAS Inhibitors. JAMA Intern Med.2025;e250686. https://doi.org/10.1001/jamainternmed.2025.0686
309.
Luo X, XuJ, Zhou S, Xue C, Chen Z, Mao Z. Influence of SGLT2i and RAASi and TheirCombination on Risk of Hyperkalemia in DKD: A Network Meta-Analysis. ClinJ Am Soc Nephrol CJASN. 2023;18:1019–30. https://doi.org/10.2215/CJN.0000000000000205
310.
Nie S, LiY, Sun Y, Chen S, Shao X, Pang M, u. a. Discontinuation of Renin-Angiotensin SystemInhibitors during Acute Kidney Injury Episode and All-Cause Mortality: TargetTrial Emulation Studies. J Am SocNephrol JASN. 2025; https://doi.org/10.1681/ASN.0000000775
311.
Optimizationof RAASi Therapy Toolkit [Internet]. Int. Soc. Nephrol. [zitiert27. Juli 2025]. https://www.theisn.org/initiatives/toolkits/raasi-toolkit/.Zugegriffen 27 Juli 2025
312.
SolomonSD, McMurray JJV, Anand IS, Ge J, Lam CSP, Maggioni AP, u. a. Angiotensin-Neprilysin Inhibitionin Heart Failure with Preserved Ejection Fraction. N Engl J Med. 2019;381:1609–20. https://doi.org/10.1056/NEJMoa1908655
313.
Butler J,Anker SD, Lund LH, Coats AJS, Filippatos G, Siddiqi TJ, u. a. Patiromer for the management ofhyperkalemia in heart failure with reduced ejection fraction: the DIAMONDtrial. Eur Heart J. 2022;43:4362–73. https://doi.org/10.1093/eurheartj/ehac401
314.
KosiborodMN, Cherney DZI, Desai AS, Testani JM, Verma S, Chinnakondepalli K, u. a. Sodium Zirconium Cyclosilicatefor Management of Hyperkalemia During Spironolactone Optimization in PatientsWith Heart Failure. J Am Coll Cardiol. 2025;85:971–84. https://doi.org/10.1016/j.jacc.2024.11.014
315.
Tardif J‑C,Rouleau J, Chertow GM, Al-Shurbaji A, Lisovskaja V, Gustavson S, u. a. Potassium reduction with sodiumzirconium cyclosilicate in patients with heart failure. ESC Heart Fail.2023;10:1066–76. https://doi.org/10.1002/ehf2.14268
316.
Gregg LP,Navaneethan SD. Steroidal or non-steroidal MRAs: should we still enable RAASiuse through K binders? Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc- Eur Ren Assoc. 2023;38:1355–65. https://doi.org/10.1093/ndt/gfac284
317.
Packer M.Do Potassium Binders Block Both the Benefits and the Risks of MineralocorticoidReceptor Antagonists in Heart Failure?: The Four Anti-Aldosterone Myths.J Am Coll Cardiol. 2025;85:985–7. https://doi.org/10.1016/j.jacc.2025.01.011
318.
McDonaghTA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, u. a. 2021 ESC Guidelines for thediagnosis and treatment of acute and chronic heart failure. Eur Heart J.2021;42:3599–726. https://doi.org/10.1093/eurheartj/ehab368
319.
SavareseG, Izquierdo MJ, Bonanad C, Wong A, Schmitt R, Ferraro PM, u. a. Interdisciplinary recommendationsfor recurrent hyperkalaemia: Insights from the GUARDIAN-HK European SteeringCommittee. Eur Heart J Cardiovasc Pharmacother. 2025;pvaf055. https://doi.org/10.1093/ehjcvp/pvaf055
320.
Shen L,Kristensen SL, Bengtsson O, Böhm M, de Boer RA, Docherty KF, u. a. Dapagliflozin in HFrEF PatientsTreated With Mineralocorticoid Receptor Antagonists: An Analysis of DAPA-HF.JACC Heart Fail. 2021;9:254–64. https://doi.org/10.1016/j.jchf.2020.11.009
321.
FerreiraJP, Zannad F, Butler J, Filipattos G, Ritter I, Schüler E, u. a. Empagliflozin and serum potassiumin heart failure: an analysis from EMPEROR-Pooled. Eur Heart J. 2022;43:2984–93. https://doi.org/10.1093/eurheartj/ehac306
322.
ArmstrongPW, Pieske B, Anstrom KJ, Ezekowitz J, Hernandez AF, Butler J, u. a. Vericiguat in Patients with HeartFailure and Reduced Ejection Fraction. N Engl J Med. 2020;382:1883–93. https://doi.org/10.1056/NEJMoa1915928
323.
HironakaJ, Okada H, Osaka T, Hashimoto Y, Kobayashi G, Tanaka M, u. a. Non-inferiority of sodiumzirconium cyclosilicate versus potassium-restricted diet in achievingnormokalaemia in patients with type 2 diabetesmellitus: protocol for a multicentre,open-label, randomised controlled, two-arm clinical trial (SILVERSTAR study).British Medical Journal Publishing Group; 2025 [zitiert 27. Juli 2025]; https://doi.org/10.1136/bmjopen-2024-089564
324.
SebastianA, Schambelan M, Sutton JM. Amelioration of hyperchloremic acidosis withfurosemide therapy in patients with chronic renal insufficiency and type 4renal tubular acidosis. Am J Nephrol. 1984;4:287–300. https://doi.org/10.1159/000166827
325.
Palmer BF,Clegg DJ. Electrolyte and Acid-Base Disturbances in Patients with DiabetesMellitus. N Engl J Med. 2015;373:548–59. https://doi.org/10.1056/NEJMra1503102
326.
SebastianA, Schambelan M, Lindenfeld S, Morris RC. Amelioration of metabolic acidosiswith fludrocortisone therapy in hyporeninemic hypoaldosteronism. N Engl J Med.1977;297:576–83. https://doi.org/10.1056/NEJM197709152971104
327.
Hahner S,Ross RJ, Arlt W, Bancos I, Burger-Stritt S, Torpy DJ, u. a. Adrenal insufficiency. Nat RevDis Primer. 2021;7:19. https://doi.org/10.1038/s41572-021-00252-7
328.
Zieg J,Thomasová D, Libik M, Sumnik Z, Bockenhauer D. Hyperkalaemic acidosis: bloodpressure is the diagnostic clue. Pediatr Nephrol Berl Ger. 2025;40:967–70. https://doi.org/10.1007/s00467-024-06590-4
329.
BandhakaviM, Wanaguru A, Ayuk L, Kirk JM, Barrett TG, Kershaw M, u. a. Clinical characteristics andtreatment requirements of children with autosomal recessivepseudohypoaldosteronism. Eur J Endocrinol. 2021;184:K15–20. https://doi.org/10.1530/EJE-20-0152
330.
FurulandH, McEwan P, Evans M, Linde C, Ayoubkhani D, Bakhai A, u. a. Serum potassium as a predictor of adverse clinicaloutcomes in patients with chronic kidney disease: new risk equations using theUK clinical practice research datalink. BMC Nephrol. 2018;19:211. https://doi.org/10.1186/s12882-018-1007-1
331.
Davis J,Israni R, Mu F, Cook EE, Szerlip H, Uwaifo G, u. a. Inpatient management andpost-discharge outcomes of hyperkalemia. Hosp Pract 1995. 2021;49:273–9. https://doi.org/10.1080/21548331.2021.1925554
332.
Jun H‑R,Kim H, Lee S‑H, Cho JH, Lee H, Yim HW, u. a. Onset of Hyperkalemia followingthe Administration of Angiotensin-Converting Enzyme Inhibitor or Angiotensin II Receptor Blocker. CardiovascTher. 2021;2021:5935149. https://doi.org/10.1155/2021/5935149
333.
Crop MJ,Hoorn EJ, Lindemans J, Zietse R. Hypokalaemia and subsequent hyperkalaemia inhospitalized patients. Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc- Eur Ren Assoc. 2007;22:3471–7. https://doi.org/10.1093/ndt/gfm471
334.
JønssonSS, Sørensen SA, Krøgh ST, Melgaard D, Søgaard P, Søndergaard MM, u. a. Short-term prognosis of changesin plasma potassium following an episode of hyperkalaemia in patients withchronic heart failure. Eur J Intern Med. 2023;118:82–8. https://doi.org/10.1016/j.ejim.2023.07.031
335.
Hutter T,Collings TS, Kostova G, Karet Frankl FE. Point-of-care and self-testing forpotassium: recent advances. Sens Diagn. 2022;1:614–26. https://doi.org/10.1039/d2sd00062h
336.
BamforthRJ, Ferguson TW, Tangri N, Rigatto C, Collister D, Komenda P. Cost-Utility ofReal-Time Potassium Monitoring in United States Patients ReceivingHemodialysis. Kidney Int Rep. 2024;9:3226–35. https://doi.org/10.1016/j.ekir.2024.08.007
337.
Kuo W‑H,You H‑L, Huang W‑T, Lee Y‑T, Chiou TT‑Y, Ng H‑Y, u. a. Incidence, characteristics andoutcomes among inpatient, outpatient and emergency department with reportedhigh critical serum potassium values. Clin Chem Lab Med. 2021;59:1231–7. https://doi.org/10.1515/cclm-2020-1476
338.
DrumhellerBC, Tuffy E, Gibney F, Stallard S, Siewers C, Korvek S. Severe bradycardia fromsevere hyperkalemia: Patient characteristics, outcomes and factors associatedwith hemodynamic support. Am J Emerg Med. 2022;55:117–25. https://doi.org/10.1016/j.ajem.2022.03.007
339.
An JN, LeeJP, Jeon HJ, Kim DH, Oh YK, Kim YS, u. a. Severe hyperkalemia requiringhospitalization: predictors of mortality. Crit Care Lond Engl.2012;16:R225. https://doi.org/10.1186/cc11872